Empleo de extractos fenólicos para el control de patógenos postcosecha de frutas
Entre las principales causas del deterioro de las frutas está el crecimiento fúngico. La aplicación de fungicidas sintéticos representa cada vez más un rechazo por parte del consumidor final, haciendo necesario la búsqueda de alternativas como las sustancias antifúngicas de carácter natural. Los compuestos fenólicos se caracterizan por mostrar propiedades antimicrobianas y, es por ello, que pueden representar una alternativa real. Así, subproductos vegetales con un alto contenido fenólico pueden ser aprovechados como fuente natural de estos compuestos con propiedades antifúngicas. Los resultados obtenidos en este trabajo mostraron que el extracto de orujo de uva presentó una elevada actividad antifúngica frente a levaduras, mientras que el extracto de alpeorujo se caracterizó por limitar el crecimiento de Botrytis cinerea, Monilia laxa y Alternaria alternata. Por lo tanto, estos extractos podrían ser una alternativa adecuada a los fungicidas de síntesis para el control de patógenos postcosecha durante los largos periodos de conservación de la fruta.
España es el mayor productor y exportador de fruta en la Unión Europea y está situado entre los tres principales exportadores a nivel mundial. Además, en los últimos años, el consumo de frutas y hortalizas se ha incrementado debido principalmente a que los consumidores son cada vez más conscientes de la relación entre dieta y salud. Por otro lado, la inocuidad o seguridad de los alimentos es uno de los principales problemas mundiales de salud pública, ya que es necesario garantizar alimentos libres de patógenos, toxinas y residuos fitosanitarios. Sin embargo, la fruta en general se caracteriza por tener una vida útil corta después de su recolección, debido en gran parte al avance de los procesos de maduración, lo que dificulta su exportación a mercados lejanos. Hoy en día, las pérdidas de frutas y hortalizas son bastante elevadas, alcanzando valores entorno al 25% de la producción en países industrializados y más del 50% en países en desarrollo, si las condiciones de almacenamiento no son óptimas.
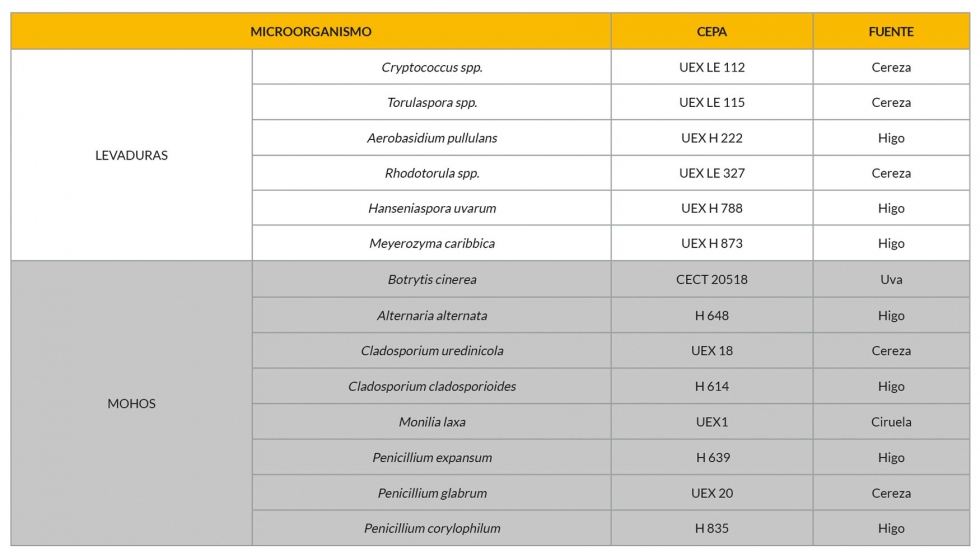
Dentro de estas pérdidas, las podredumbres de frutos causadas por el desarrollo fúngico son las más relevantes, ya que generan rechazo del producto tanto por parte de los importadores como de los consumidores finales. Entre los principales mohos causantes de podredumbre se encuentran varias especies pertenecientes a los géneros Penicillium, Botrytis, Monilia, Cladosporium, Rhizopus, Mucor y Alternaria (Barkai-Goland, 2001). Además, las levaduras forman parte de la flora natural de las frutas, y se ha determinado que su presencia en elevado número influye directamente en la pérdida de calidad del producto (Ragaert y col., 2006).

En la industria transformadora de productos de la agricultura se generan elevadas cantidades de subproductos que en muchas ocasiones son difíciles de gestionar. Muchos de estos subproductos se caracterizan por presentar un elevado contenido de compuestos fenólicos a los cuales se le atribuyen importantes actividades antioxidantes y antimicrobianas (Brenes y col., 2016). Estas propiedades son de gran interés y podrían potenciar el desarrollo de vías alternativas para su reutilización.
Por todo ello, el objetivo de este trabajo fue evaluar el potencial antifúngico de extractos fenólicos de alpeorujo y orujo de uva frente a las principales especies de mohos y levaduras causantes de podredumbre en fruta, para su potencial reutilización como fuente de compuestos antimicrobianos naturales.
Material y métodos
Preparación de los extractos polifenólicos
Para la obtención de los extractos, el alpeorujo fue obtenido tras la extracción del aceite procedente de las variedades de aceituna 'Cornezuelo' y 'Manzanilla', y el orujo de uva de frutos de las variedades 'Pinot Noir', 'Syrah', 'Garnacha', 'Cabernet' 'Sauvignon' y 'Tempranillo'. Los subproductos se secaron en una estufa de ventilación forzada a 45 °C y, posteriormente, se molieron hasta obtener un tamaño de partícula inferior a 2 mm. La extracción de los compuestos se realizó con una solución extractora compuesta por etanol, agua destilada y ácido clorhídrico (80:19:1 v/v), manteniéndose en oscuridad y agitación durante 2 h a temperatura ambiente. Posteriormente, se procedió a la eliminación del etanol en un evaporador rotativo y a su purificación mediante columnas C18 Sep-Pak (Thermo Scientific). La concentración de fenoles de solución acuosa obtenida se determinó mediante el método Folin-Ciocalteu, tal y como describe Schlesier y col. (2002).
Actividad antifúngica
Para determinar la actividad antimicrobiana frente a levaduras se empleó un turbidómetro automático Bioscreen C (Labsystems, Finlandia) con un filtro de banda amplia (OD 420 a 580 nm) para la medición de la turbidez del medio. En cada pocillo se añadió medio YPD suplementado con diferentes concentraciones de fenoles (0-1,5 g/L) de cada extracto (EAP o EOU), inoculándose con un 0,5% (v/v) de una suspensión de levaduras a 108 ufc/mL, crecida durante 18 h a 25 °C. Se realizó un ensayo control inoculando cada microorganismo sin la adición del extracto polifenólico. A continuación, los cultivos se incubaron a 25°C durante 48 h. El efecto inhibidor del crecimiento se determinó mediante la comparación de las lecturas de turbidez de cada levadura a las diferentes concentraciones de fenoles, con las obtenidas en ausencia de compuestos fenólicos. El porcentaje de inhibición se calculó con la siguiente fórmula:
% de inhibición = (DO ensayo-DO control /DO ensayo) x100
DO control: densidad óptica del crecimiento de la levadura ensayada en ausencia de compuestos fenólicos.
DO ensayo: densidad óptica del crecimiento de la levadura ensayada en presencia de compuestos fenólicos.
Por otro lado, para estudiar el efecto inhibidor del extracto acuoso polifenólico sobre los mohos, se analizó su influencia sobre el crecimiento radial del micelio de las 8 cepas mohos (Tabla 1). Previamente al ensayo, los mohos fueron crecidos en agar PDA a 25 °C hasta su esporulación. Las esporas fueron recogidas lavando la superficie con una solución estéril de Tween 80 al 0,05%. A continuación, se cuantificó el número de esporas de cada cepa con un microscopio óptico y cámara de Neubauer (hemocitómetro).
Para determinar el efecto inhibidor de cada extracto sobre los diferentes mohos estudiados se prepararon placas de agar PDA que contenían concentraciones de EAP entre 0 y 1,5 g/L. Una vez solidificadas las placas de PDA, conteniendo las diferentes concentraciones del extracto, se inocularon asépticamente en el centro de la placa con 10 µL de una suspensión de 105 esporas/mL. Debido a su incapacidad para esporular, en el caso de Monilia laxa y Alternaria alternata H648, le ensayo se realizó inoculando en el centro de la placa un trozo de agar de 6 mm de diámetro de micelio previamente crecido durante 7 días. Las placas de PDA de agar se incubaron a 25 °C durante 7 días, midiendo por duplicado en cada placa el diámetro de crecimiento del moho a los 2, 4, y 7 días de incubación. El porcentaje de inhibición del crecimiento radial del moho diana se calculó según la siguiente fórmula:
% de inhibición = (DC-DT) / DC x 100
DC: diámetro de crecimiento del moho en PDA agar sin tratar (mm)
DT: diámetro de crecimiento del moho en PDA conteniendo la solución de polifenoles (mm)
Todos los experimentos se realizaron por duplicado, a partir de los dos extractos fenólicos diferentes, y en cada experimento cada ensayo fue realizado por triplicado.
Resultados y discusión
La actividad antifúngica de extractos fenólicos acuosos obtenidos de subproductos de la industria agraria, alpeorujo y orujo de uva, fue evaluada frente a levaduras y mohos causantes de alteración en fruta. En la Figura 1 se muestra la actividad antimicrobiana de ambos extractos a concentraciones variables, entre 0,5 g/l y 1,5 g/l, frente a seis especies de levaduras aisladas de fruta. La capacidad inhibitoria del EOU fue claramente más efectiva en el control del crecimiento de las seis levaduras estudiadas. La inoculación en el medio de cultivo de concentraciones superiores a 1 g/L de EOU mostró porcentajes de inhibición superiores al 80% frente a todas las levaduras. De hecho, a una concentración de 1,5 g/l el EOU inhibió totalmente el crecimiento de 4 de las 6 cepas de levaduras, Cryptococcus spp., Torulaspora spp., Rhodotorula spp. y Hanseniospora uvarum. Sin embargo, la capacidad de inhibición del EAP fue significativamente inferior incluso a la máxima concentración de 1,5 g/l, con valores que variaron entre el 45-65%, dependiendo la cepa de levadura.
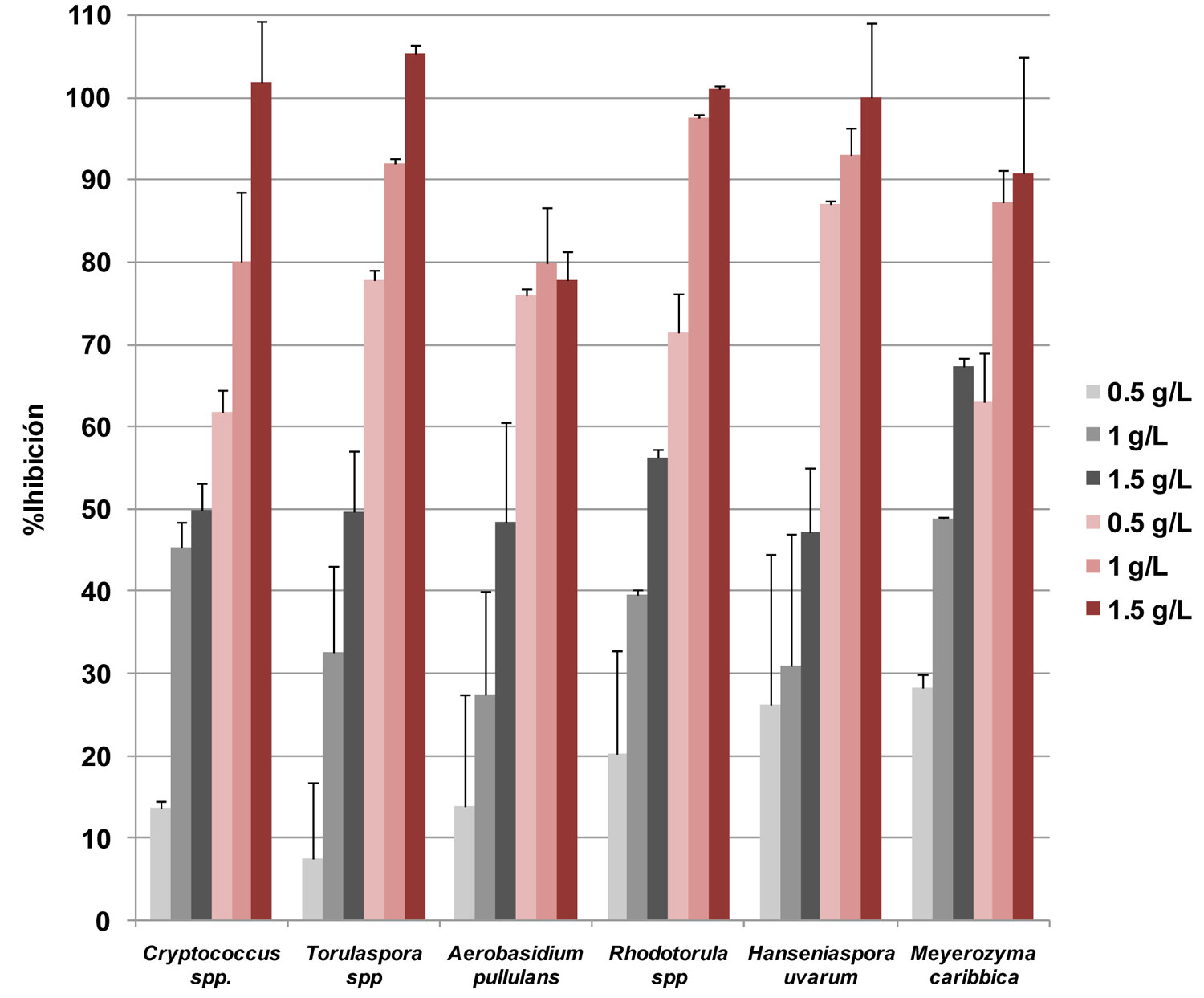
Los estudios del efecto antimicrobiano de extractos fenólicos de subproductos de almazara o de la industria vitivinícola sobre levaduras son escasos y se han centrado principalmente frente a especies de importancia clínica como las pertenecientes al género Candida spp. (Bouaziz y col., 2008). Por otro lado, algunos autores han estudiado la capacidad antifúngica de compuestos fenólicos puros presentes en estos subproductos en concentraciones importantes. Concretamente, Jung y col. (2007) estudió la actividad antifúngica del resveratrol frentre a C. albicans, mientras que Pastorkova y col. (2013) analizó la capacidad inhibitoria de la luteolina frente a diversas especies de levaduras entre las que se encontraba Hanseniaspora uvarum. Sería interesante analizar más en profundidad los extractos empleados en el presente estudio, para determinar el o los compuestos responsables de su actividad antimicrobiana.
Por otro lado, en relación a la actividad antifúngica frente a mohos patógenos postcosecha, en la Figura 2 se muestra el potencial inhibitorio de los extractos fenólicos de alpeorujo y orujo de uva frente a 8 cepas de mohos pertenecientes a las principales especies causantes de podredumbre en fruta (Tabla 1). El EAP mostró un efecto marcado sobre tres de las especies de mohos responsables de importantes podredumbres postcosecha y sobre los que se centra la búsqueda de sustancias antifúngicas, Botrytis cinerea CECT 20518, Monilia laxa UEX1 y Alternaria alternata H648. El crecimiento de B. cinerea fue inhibido en valores entorno al 45% a concentraciones superiores a 1 g/l (Fig. 2 A), mientras que un resultado similar fue obtenido frente a A. alternata a 1.5 g/l (Fig. 2C). Estudios previos con extractos fenólicos de subproductos de almazara han mostrado el potencial antifúngico de compuestos fenólicos frente a B. cinerea (Yangui y col., 2010; Leontopoulos y col., 2015). A reseñar, que el efecto del EAP frente a M. laxa, causante de la podredumbre marrón en fruta de hueso, fue considerablemente superior, inhibiendo a una concentración de 1,5 g/l totalmente el crecimiento tras 2 días de ensayo y entorno al 60% en días posteriores (Fig. 2 B). Contrariamente a los resultados obtenidos frente a levaduras, el EOU mostró una menor capacidad para el control del crecimiento fúngico de las especies de mohos estudiadas. Este extracto sólo mostró una capacidad inhibitoria destacable frente a A. alternata y C. cladosporioides, con valores de aproximadamente 60% y 40%, respectivamente, a los 4 y 7 días de estudio. Estos resultados difieren de los obtenidos por Mendoza y col. (2013), los cuales mostraron cierta actividad de EOU frente a B. cinerea, aunque la actividad antifúngica era variable dependiendo del método de extracción utilizado. En cuanto al resto de especies fúngicas estudiadas, pertenecientes a los géneros Penicillium spp. y Cladosporium spp. el efecto antimicrobiano de ambos extractos fue limitado (Fig. 2).
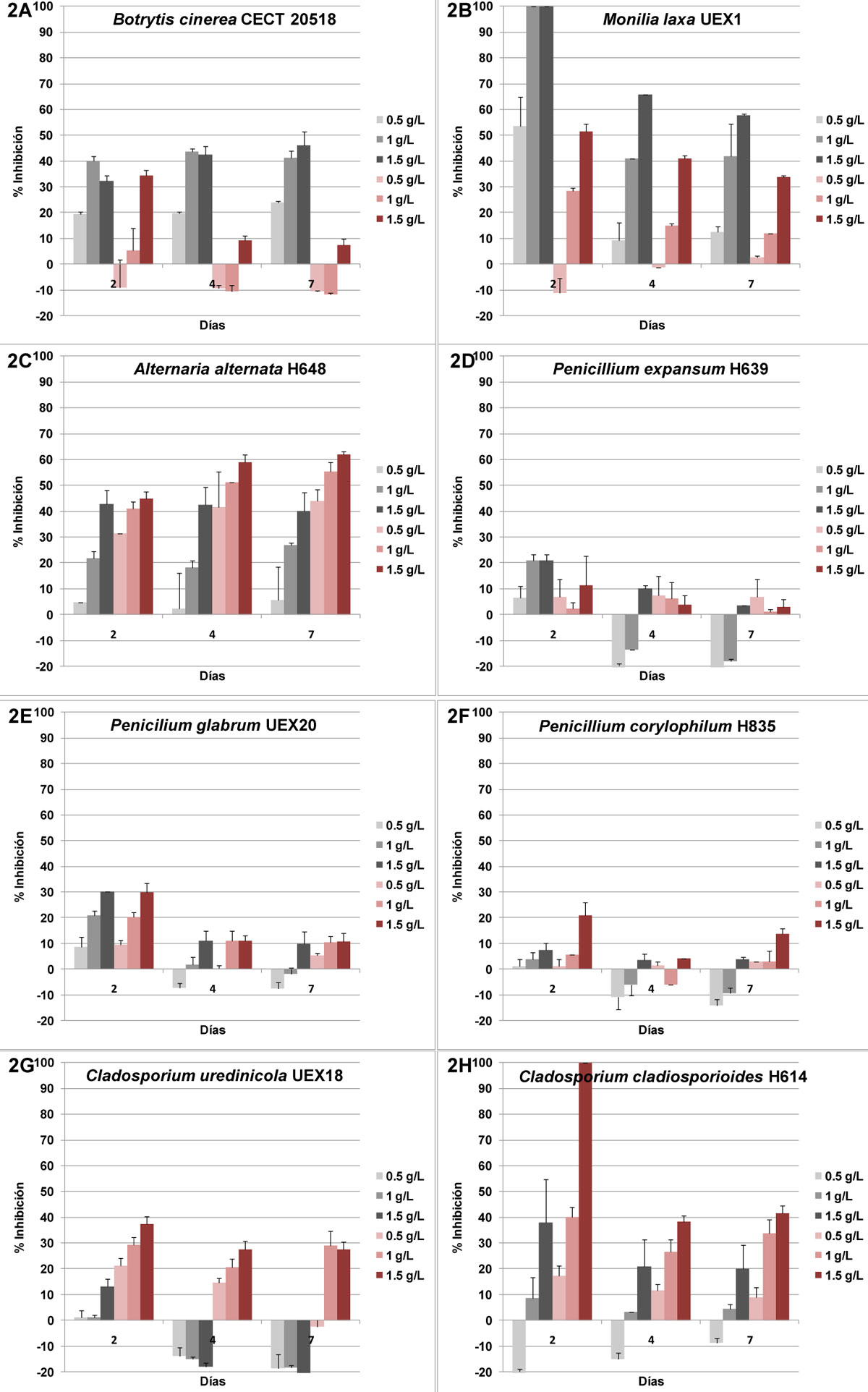
En conclusión, el extracto de orujo de uva mostró una elevada actividad antifúngica frente a levaduras, mientras que el extracto de alpeorujo mostró una moderada capacidad de inhibir el crecimiento de levaduras y frente a tres de los principales mohos causantes de podredumbre en fruta, Botrytis cinerea, Monilia laxa y Alternaria alternata. Por lo tanto, aunque estudios in vivo son necesarios, estos compuestos podrían ser una alternativa natural a los fungicidas químicos en tratamientos postcosecha para incrementar la vida útil de las frutas.
Agradecimientos
Este trabajo ha sido financiado por la ayuda a grupos de investigación de la Junta de Extremadura y fondos FEDER (ref. GR15166).
Referencias bibliográficas
- Barkai-Goland, R. 2001. Postharvest diseases of fruit and vegetables. Development and control. Ed. Elsevier. Amsterdam, The Nedherlands.
- Brenes, A., Viveros, A., Chamorro, S., Arija, I. 2016. Use of polyphenol-rich grape by-products in monogastric nutrition. A review. Animal Feed Science and Technology, 211, 1-17.
- Bouaziz, M., Lassoued, S., Bouallagui, Z., Smaoui, S., Gargoubi, A. Dhouib, A. Sayadi, S. 2008. Synthesis and recovery of high bioactive phenolics from table-olive brine process wastewater. Bioorganic & Medicinal Chemistry, 16: 9238-9246.
- Jung, H. J., Seu, Y. B., Lee, D. G. 2007. Candicidal action of resveratrol isolated from grapes on human pathogenic yeast C. albicans. Journal of microbiology and biotechnology, 17(8), 1324-1329.
- Leontopoulos, S.V., Giavasis, I., Petrotos, Kokkora, M., Makridisa, Ch. 2015. Effect of Different Formulations of Polyphenolic Compounds Obtained from OMWW on the Growth of Several Fungal Plant and Food Borne Pathogens. Studies in vitro and in vivo. Agriculture and Agricultural Science Procedia 4: 327-337.
- Mendoza, L., Yañez, K., Vivanco, M., Melo, R., Cotoras, M. 2013. Characterization of extracts from winery by-products with antifungal activity against Botrytis cinerea. Industrial crops and products, 43, 360-364.
- Pastorkova, E., Zakova, T., Landa, P., Novakova, J., Vadlejch, J., Kokoska, L. 2013. Growth inhibitory effect of grape phenolics against wine spoilages yeast and acetic acid bacteria. International Journal of Food Microbiology 161: 209-213.
- Ragaert, P., Devlieghere, F., Loos, S., Dewulf, J., Van Langenhove, H., Foubert, I., Vanrolleghem, P.A. & Debevere J. 2006. Role of yeast proliferation in the quality degradation of strawberries during refrigerated storage. International Journal of Food Microbiology 108: 42-50.
- Schlesier, K., Harwat, M., Bohm, V., Bitsch, R. 2002. Assessment of antioxidant activity by using different in vitro methods. Free Radical Research 36: 177-187.
- Yangui, T., Sayadi, S., Rhouma, A., Dhouib, A. 2010. Potential use of hydroxytyrosol-rich extract from olive mill wastewater as a biological fungicide against Botrytis cinerea in tomato. Journal of Pest Science 83: 437-445.