Uso de sensores de reflectancia para caracterizar el estado nutricional de nitrógeno en espinaca

La producción intensiva de cultivos de hortalizas está generalmente asociada con pérdidas considerables de N por lixiviación que pueden dar lugar a contaminación de acuíferos y aguas superficiales (Pratt, 1984). Las cantidades excesivas de fertilizantes nitrogenados, la baja eficiencia en la absorción de los mismos por el cultivo y el exceso de riego son frecuentes en estos sistemas de producción (Pratt, 1984; Thompson et al., 2007). Muchas de las zonas donde se concentra la producción de hortalizas en España han sido declaradas 'Zonas vulnerables a la contaminación por nitratos de origen agrícola' (ZVN) según la directiva comunitaria 91/676/CEE. Hasta ahora, la Directiva sobre nitratos no ha sido fuertemente implantada en países del sur de Europa, en contraste con otros países del noroeste como Bélgica, Alemania, Holanda o Dinamarca. Adicionalmente, en hortalizas de hoja el Reglamento europeo 1258/2011 establece las cantidades máximas permitidas de nitratos en hoja de espinaca y lechuga, tanto para consumo en fresco como para congelado. Por todo ello, se hace necesario desarrollar métodos eficaces de gestión del N en sistemas de cultivo de hortalizas, que minimicen las pérdidas de N sin reducir la producción.
Giller et al. (2004) propusieron un método de gestión del N en el que se combinan métodos prescriptivos y correctivos. Los métodos prescriptivos realizan un plan de gestión del N optimizado. Determinan antes de la siembra la cantidad y el momento de las aplicaciones durante el ciclo del cultivo, basado en la respuesta esperada del cultivo al fertilizante N. Entre los métodos prescriptivos, uno de los más prometedores son los modelos de simulación. Los métodos correctivos emplean herramientas de diagnóstico que estiman el estado nutricional en N del cultivo, para realizar correcciones en la fertilización en determinados estados fenológicos que garanticen el estado óptimo del cultivo durante todo su ciclo. Los métodos disponibles en la actualidad para caracterizar el estado nutricional de cultivos son numerosos, desde medidas agronómicas tradicionales hasta otros más sofisticados que han surgido a raíz de la disponibilidad de nuevas tecnologías que han podido ser aplicadas a la agricultura. Entre los tradicionales se encuentra el análisis foliar de N total, método muy establecido en la comunidad científica internacional como referencia para comparar otros indicadores.
Sin embargo, el contenido de N total en valor absoluto no da información definitiva sobre el estado nutricional, ya que disminuye a lo largo del ciclo del cultivo. Lemaire et al. (2008) han propuesto el Indice de Nutrición Nitrogenada (Nitrogen Nutrition Index, NNI) basado en la curva crítica de dilución del N ('Critical Nitrogen Curve', CNC) propuesta por Greenwood et al. (1990). La CNC indica la relación entre el %N y la biomasa del cultivo y representa el valor mínimo de %N que el cultivo debe tener en cada momento del ciclo para no reducir su biomasa por déficit de N. En los últimos años se han desarrollado sensores que incorporan nuevas tecnologías para determinar el estado de N de cultivos basadas en las propiedades ópticas de las hojas, las cuales están relacionadas con su contenido de N. Las propiedades ópticas reflejan su estado nutricional, indicando por tanto el grado de suficiencia o deficiencia en N. Estos sensores son diversos y difieren en el posicionamiento de los mismos respecto al cultivo (proximales o remotos) y en las longitudes de onda a las cuales se realizan las determinaciones (multiespectrales o hiperespectrales). En los últimos años se están llevando a cabo numerosas investigaciones para estudiar el estado nutricional y determinar las dosis óptimas de fertilizante N en diversos cultivos mediante el uso de sensores ópticos (Fox and Walthall, 2008; Samborski et al., 2009; Tremblay et al., 2012; Thompson et al., 2017).

Los sensores proximales de reflectancia multiespectrales se colocan a poca distancia del cultivo (0,4 3 m) y miden la radiación de diferentes longitudes de onda reflejada por el mismo, que suelen estar en las bandas del verde, rojo (0,6-0,7 µm; región de absorción de la clorofila), rojo lejano e infrarrojo cercano (0,7-1,3 µm; bandas de no-absorción). Los sensores hiperespectrales miden la reflectancia en bandas muy estrechas del espectro, de forma casi continua, desde el visible al infrarrojo (400-2.500 nm), lo que supone una ventaja frente a los sensores que solo utilizan 3-6 longitudes de onda. A partir de las lecturas de reflectancia a diferentes longitudes de onda se han derivado multitud de ecuaciones matemáticas (Indices de Vegetación, IV), que incluyen cocientes entre bandas, diferencias normalizadas, combinaciones lineales de bandas y combinaciones optimizadas de bandas (Tucker, 1979). Los sensores hiperespectrales ofrecen la posibilidad de cálculo de un mayor número de índices que los multiespectrales debido al mayor número de medidas en un rango mucho más amplio del espectro.
Índices de vegetación en espinaca
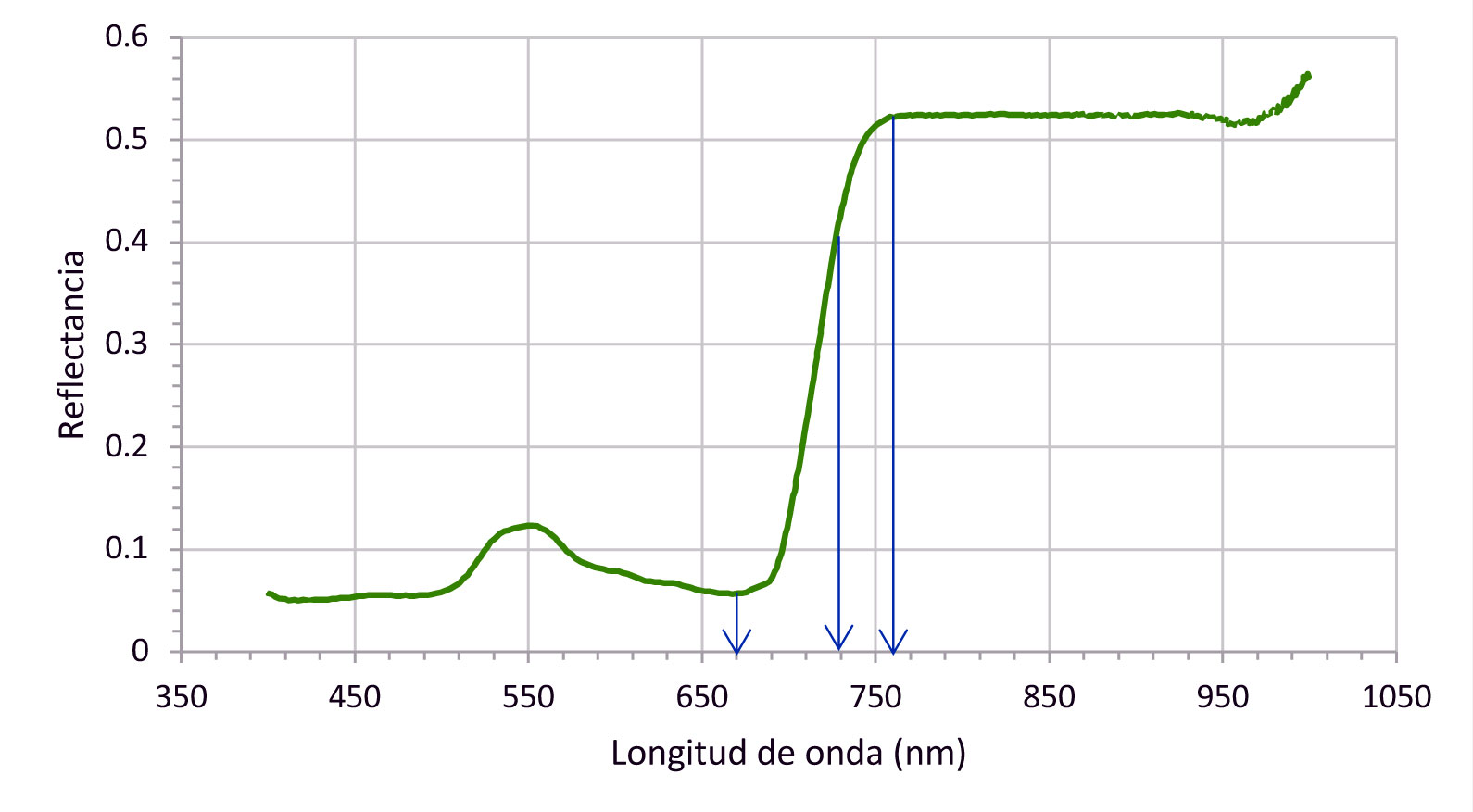
La Figura 1 muestra un ejemplo de una curva de reflectancia de una hoja de espinaca a longitudes de onda entre 400 y 1.000 nm. La mayor reflectancia en la zona del verde (550 nm) se debe a la baja absorción de la clorofila a estas longitudes de onda. Debido a la relación entre contenido de N y de clorofila en multitud de especies, la reflectancia a 550 nm es sensible a cambios en el estado nutricional del N en la planta. Otra zona de interés del espectro es la situada entre la zona de fuerte absorción de luz roja (670 nm) por la clorofila y de fuerte reflexión cerca de las longitudes de onda del infrarrojo (780 nm). Esta zona se conoce como red edge y en la Figura 1 se puede observar el rápido y drástico incremento de la reflectancia en este intervalo de longitudes de onda. La zona red edge se desplaza ligeramente hacia mayores longitudes de onda a medida que el contenido de clorofila aumenta (Gates et al., 1965). Por tanto, los índices de vegetación que se han estudiado hasta ahora han estado basados principalmente en medidas de reflectancia a estos intervalos de longitudes de onda, que son sensibles a un cambio en el estado nutricional de N del cultivo.
La mayoría de los estudios publicados se han realizado en cultivos extensivos, a fin de desarrollar índices que sirviesen como herramienta para manejar adecuadamente la fertilización, especialmente de cobertera. Sin embargo, hay pocos estudios en hortalizas de hoja a pesar de la importancia de controlar la fertilización en estos cultivos, tradicionalmente fuertemente fertilizados, lo que supone un alto riesgo de acumulación excesiva de nitratos en hoja y de contaminación del medio ambiente.
A continuación se presentan datos de espinaca para congelado de diferentes estudios realizados en el sur de España, orientados a determinar los mejores índices de vegetación (IV) que caractericen su estado nutricional de N. Estos datos incluyen un amplio intervalo de contenido en N obtenido mediante aplicaciones crecientes de fertilizante nitrogenado, desde la no fertilización hasta el 150% de la dosis tradicionalmente usada por los agricultores de las zonas de estudio. A lo largo del ciclo de cada cultivo se han usado dos sensores para tomar medidas de reflectancia, uno multiespectral (RapidScan CS45, Holland Scientific) que toma medidas a nivel de cubierta a 3 longitudes de onda (670, 730 y 780 nm) y otro hiperespectral (CI-710, CID Bio-Science) que mide en hojas individuales en bandas de 0,22 nm entre 400 y 950 nm. El uso del sensor hiperespectral por tanto, permite el cálculo de un mayor número de índices, ya que proporciona medidas de reflectancia a un número de longitudes de onda mucho mayor que el sensor multiespectral.
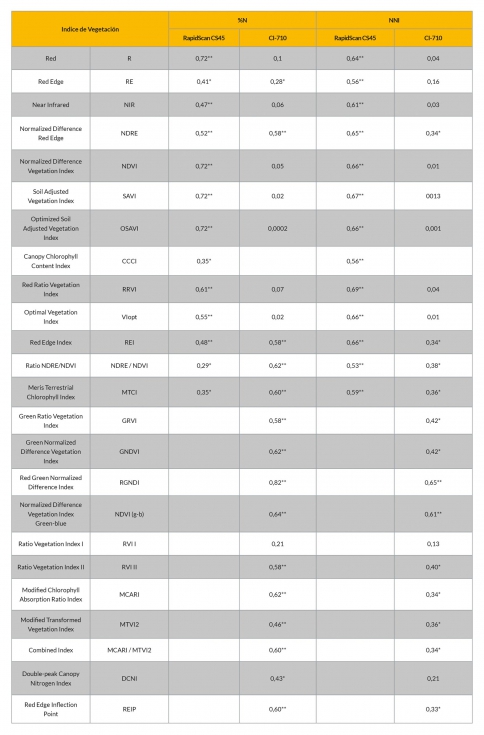
Se seleccionaron índices que resultaron ser buenos estimadores del contenido de N en planta en otros cultivos. En la Tabla 1 se muestran los 10 índices de vegetación calculados con las medidas del sensor multiespectral (RapidScan CS45). Con las medidas del sensor hiperespectral (CI-710) se calcularon, además de los índices recogidos en la tabla 1, 11 índices adicionales más (Tabla 2). Paralelamente, se determinó el %N en la materia seca de muestras cosechadas en las fechas de medida y se calculó el Nitrogen Nutrition Index (NNI) usando la curva crítica de N desarrollada localmente (García López, 2015). Se establecieron relaciones entre los valores de los índices calculados y el %N o el NNI, calculándose el coeficiente de determinación.
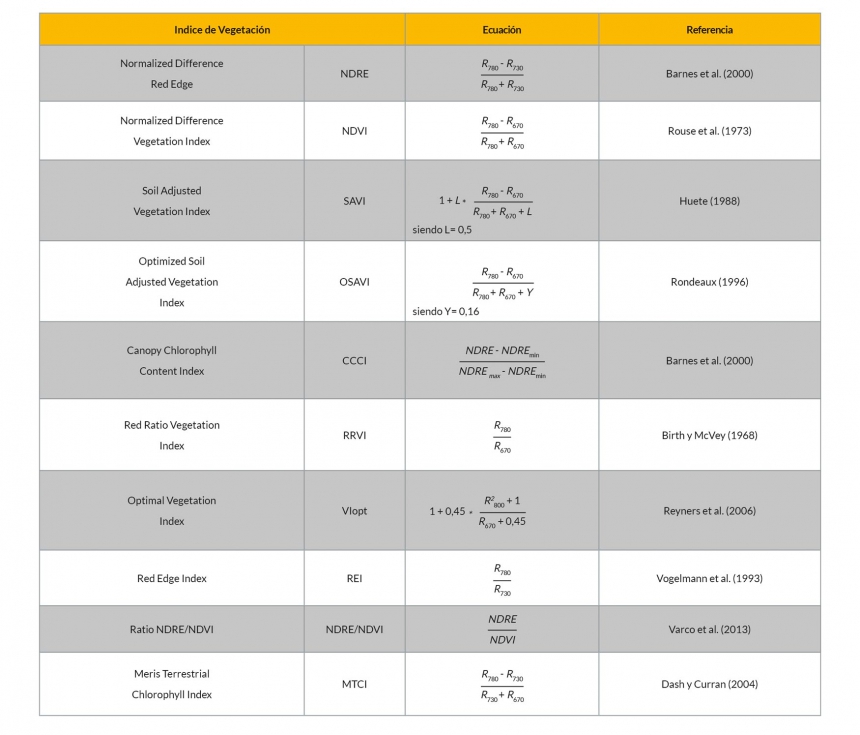
Tabla 1: Índices calculados a partir de lecturas del RapidScan CS45 a nivel de cubierta y de lecturas del espectrómetro CI-710 en hojas individuales.
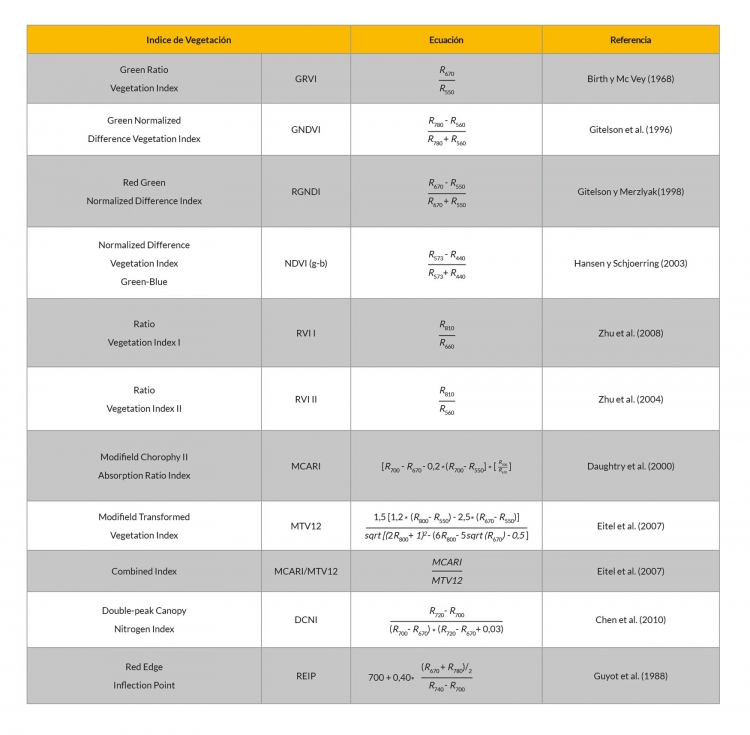
Tabla 2. Índices adicionales a los mostrados en la Tabla 1, calculados a partir de lecturas del sensor CI-710 en hojas individuales.
Los índices calculados con los valores del sensor RapidScan mostraron una mejor relación con el contenido de N en planta, expresado como %N, con mejores coeficientes de determinación que los calculados con las medidas del CI-710. Estos últimos mostraron valores de R2 de bajos a muy bajos, mientras que fueron razonablemente buenos los calculados con los valores del RapidScan CS45 (Tabla 3). De entre los demás índices calculados solo con las medidas del CI-710, algunos de ellos mostraron un alto nivel de significación (Tabla 3). Las Figuras 2a y 2b muestran la relación entre la reflectancia en el rojo (R) y el SAVI con el %N, cuando los índices se calcularon con datos del sensor multiespectral a nivel de cubierta, con coeficientes de determinación superiores a 0,71. El OSAVI, que es una optimización del SAVI, no mejoró la relación con el %N. A nivel de hoja individual, los índices calculados a partir de medidas del CI-710, RGNDI y el NVDI (g- b) fueron los que mostraron una mejor relación con el %N, con coeficientes de determinación entre 0,644 y 0,822 (Figs. 2c y 2d). Los valores negativos del RGNDI indican la mayor reflectancia en la región del verde. El nivel de significación de la relación de todos los índices calculados, tanto con medidas del RapidScan CS45 como del CI- 710, con el %N en planta se muestran en la Tabla 3.
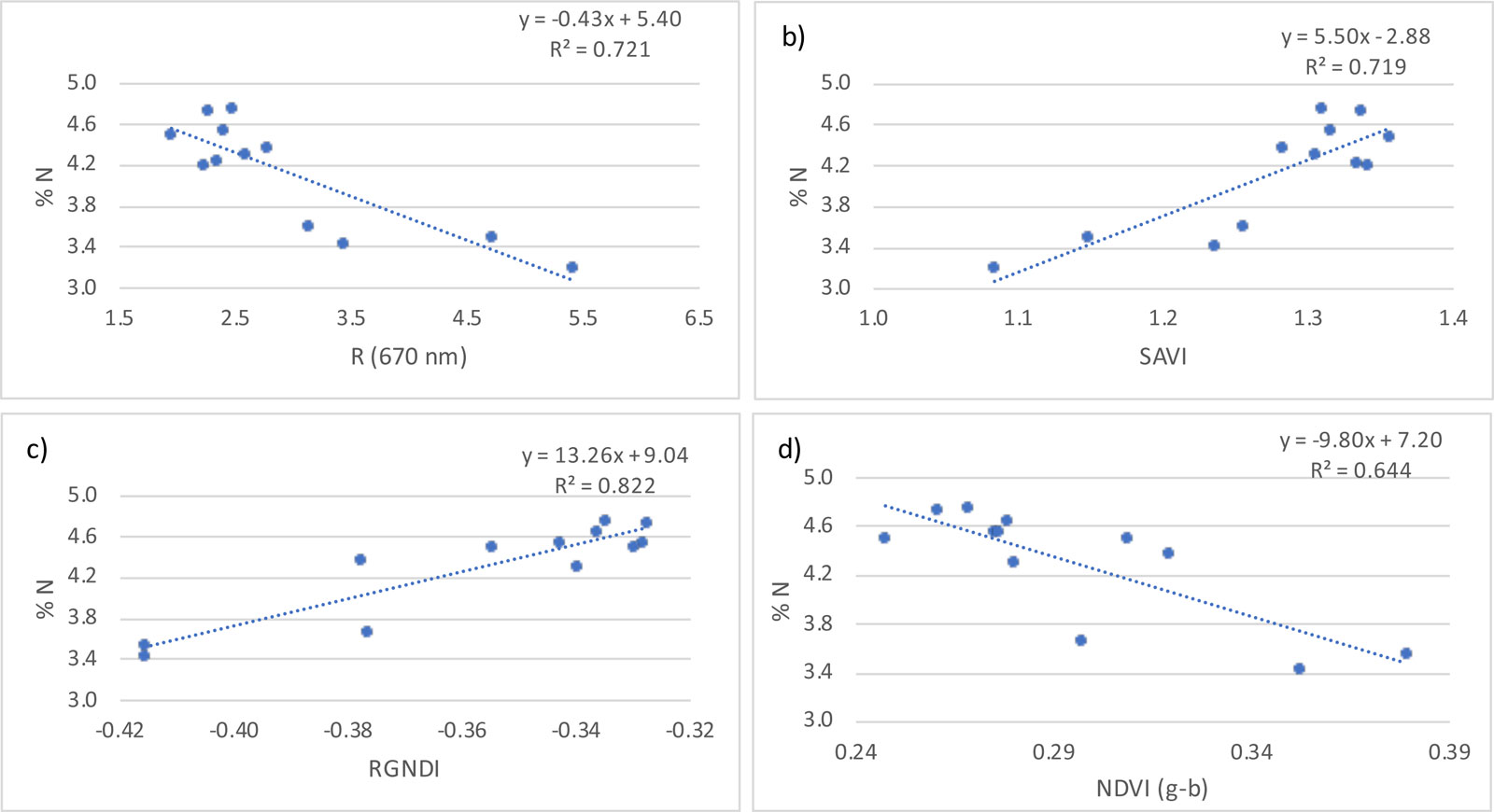
Figura 2: Relación entre los índices de vegetación indicados en la figura y el contenido de N en planta (%N). La reflectancia en el rojo (R) y el SAVI en las figuras a) y b) se calcularon con las medidas realizadas a nivel de cubierta con el RapidScan CS45, y el RGNDI y el NDVI(g-b) de las figuras c) y d) con las realizadas a nivel de hoja con el sensor C-710. Se muestran las ecuaciones y los coeficientes de determinación.
Una relación de los índices más aplicada al manejo de la fertilización nitrogenada sería cuando ésta se establece con el Nitrogen Nutrition Index (NNI), ya que el %N en planta disminuye a lo largo del ciclo. Sin embargo, el NNI indica el grado de suficiencia (NNI>1) o deficiencia (NNI<1) de N del cultivo. Cuando se relacionaron los índices estudiados con el NNI, todos los calculados a nivel de cubierta con el sensor multiespectral RapidScan CS45 mostraron una alta significación, sin embargo la significación de los calculados a partir de datos tomados con el CI-710 en hojas individuales fueron muy inferiores (Tabla 3). Posiblemente estas diferencias se deban al efecto integrador que tienen las medidas realizadas con el RapidScan CS45, las cuales se realizan sobre una superficie más o menos extensa y a nivel de cubierta, no sobre hojas individuales. En la figura 3 se muestran algunos índices de los que mostraron una mejor relación con el NNI, dos calculados a partir de medidas con el RapidScan CS45 (Figs. 3a y 3b) y otros dos calculados con medidas con el CI-710 (Figs. 3c y 3d).
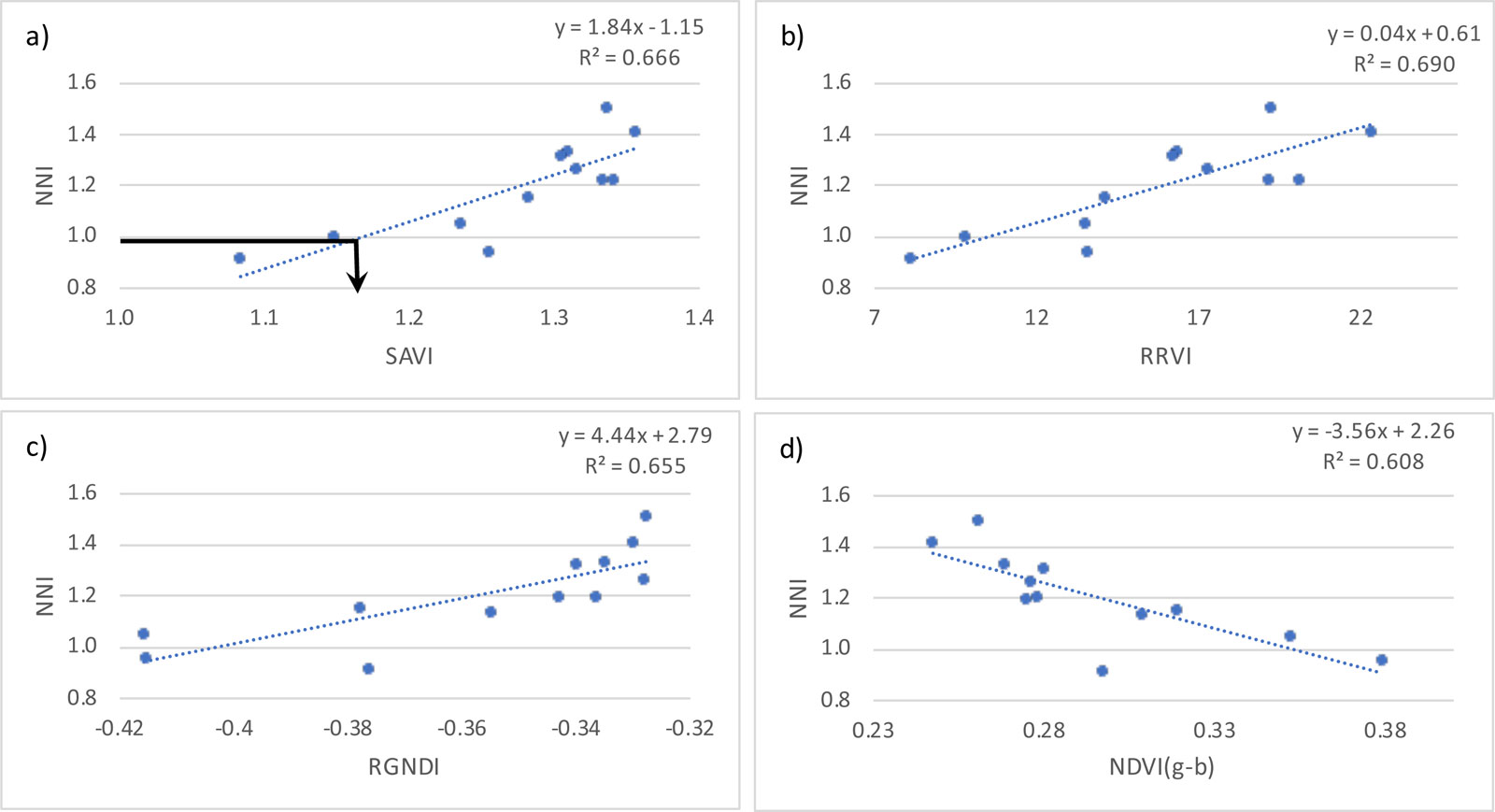
A partir de las relaciones de los IV con el NNI se pueden derivar los valores de suficiencia para cada uno de ellos. El valor de suficiencia sería el valor del IV para un NNI=1. Valores de IV superiores al de suficiencia corresponderían a valores de NNI>1 y por tanto indicarían suficiencia de N en el cultivo. Por el contrario, valores de IV inferiores al de suficiencia corresponderían a un NNI<1, indicando en este caso deficiencia de N. En la Figura 3a se muestra marcado con una flecha y a modo de ejemplo el valor de suficiencia del índice SAVI (1,17).
Una vez obtenidos los valores de suficiencia para los IV altamente relacionados con el NNI, lecturas rápidas con estos sensores nos darían información sobre el estado nutricional de N del cultivo y sobre la necesidad o no de aplicación de fertilizante nitrogenado.
El uso de medidas de reflectancia se presenta como una herramienta prometedora para el manejo adecuado de la fertilización nitrogenada en cultivos de hoja, en este caso en espinaca. A pesar del número reducido de longitudes de onda a las que miden, los sensores multiespectrales presentan ciertas ventajas frente a los hiperespectrales, principalmente la mayor facilidad de análisis de los datos y su menor precio. En la actualidad, existen en el mercado modelos comerciales que pueden ser fácilmente usados por agricultores y técnicos.
Referencias bibliográficas
- Barnes, E.M., Clarke, T.R., Richards, S.E., Colaizzi, P.D., Haberland, J., Kostrzewski, M., Waller, P., Choi, C., Riley, E., Thompson, T., Lascano, R.J., Li, H., Moran, M.S. 2000. Coincident detection of crop water stress, nitrogen status and canopy density using ground-based multispectral data. In: Robert, P.C., Rust, R.H., Larson, W.E. (Eds.). Proc. 5th Int. Conf. Precis. Agric. Bloomington, MN, USA.
- Birth, G. S., McVey, G. R. 1968. Measuring color of growing turf with a reflectance spectrophotometer. Agron. J. 60 (6), 640-643.
- Chen, P., Haboudane, D., Tremblay, N., Wang, J., Vigneault, P., Li, B. 2010. New spectral indicator assessing the efficiency of crop nitrogen treatment in corn and wheat. Remote Sens. Environ. 114, 1987-1997.
- Dash, J., Curran, P. J. 2004. The MERIS terrestrial chlorophyll index. Int. J. Remote Sens. 25(23), 5403-5413.
- Daughtry, C. S. T., Walthall, C. L., Kim, M. S., Brown de Colstoun, E., McMurtrey, J. E. 2000. Estimating corn leaf chlorophyll concentration from leaf and canopy reflectance. Remote Sens. Environ. 74, 229-239.
- Eitel, J. U. H., Long, D. S., Gessler, P. E., Smith, A. M. S. 2007. Using in-situ measurements to evaluate the new RapidEye satellite series for prediction of wheat nitrogen status. Int. J. Remote Sens. 28, 4193-4190.
- Fox, R. H., Walthall, C. L. 2008. Crop Monitoring Technologies to Assess Nitrogen Status. In: Schepers et al. (Eds.). Nitrogen in Agricultural Systems. Agronomy Monograph 49, Am. Soc. Agron., Madison, WI, USA. pp. 647-674.
- García López, M.T. 2015. Adaptación del modelo de simulacion VegSyst al cultivo de espinaca (Spinacia oleracea L.) al aire libre. Trabajo fin de Máster. Universidad de Córdoba. 33 pp.
- Gates, D.M., Keegan, H.J., Schlecter, J.C., Weidner, V.R. 1965. Spectral properties of plants. Appl. Optics 4(1), 11-20.
- Giller, K.E., Chalk, P., Doberman, A., Hammond, L., Heffer, P., Ladha, J.K., Nyamudeza, P., Maene, L., Ssali, H., Freney, J. 2004. Emerging technologies to increase the efficiency of use of fertilizer nitrogen. In: Mosier, A.R., Syers, K.J., Freney, J.R. (Eds.) Agriculture and the nitrogen cycle. Assessing the impacts of fertilizer use on food production and the environment. Island Press, Washington DC, USA. pp. 35-51.
- Gitelson, A.A., Kaufman, Y.J., Merzlyak, M.N. 1996. Use of a green channel in remote sensing of global vegetation from EOS-MODIS. Remote Sens. Environ. 58, 289-298.
- Gitelson, A. A., Merzlyak, M. N. 1998. Remote sensing of chlorophyll concentration in higher plant leaves. A3 1 Symposium of COSPAR Scientific Commission A on Synergistic Use of Multisensor Data for Land Processes at 31st COSPAR Scientific Assembly. Birmingham, UK.
- Greenwood, D. J., Lemaire, G., Gosse, G., Cruz, P., Draycott, A., Neeteson, J. 1990. Decline in percentage N of C3 and C4 crops with increasing plant mass. Ann. Botany 66 (4), 425-436.
- Guyot, G., Baret, F., Major, D. J. 1988. High spectral resolution: Determination of spectral shifts between the red and the near infrared. Int. Arch. Photogram. Remote Sens. 11, 740-760.
- Hansen, P. M., Schojoerring, J. K. 2003. Reflectance measurement of canopy biomass and nitrogen status in wheat crops using normalized difference vegetation indices and partial least squares regression. Remote Sens. Environ. 86, 542-553.
- Huete, A. 1988. A soil adjusted vegetation index (SAVI). Remote Sens. Environ. 25, 295-309.
- Lemaire, G., Jeuffroy, M., Gastal, F. 2008. Diagnosis tool for plant and crop N status in vegetative stage: Theory and practices for crop N management. Eur. J. Agron. 28, 614- 624.
- Pratt, P.F. 1984. Nitrogen use and nitrate leaching in irrigated agriculture. In: Hauk, R.D. (Ed.). Nitrogen in Crop Production. Am. Soc. Agron., Madison, WI, USA. pp. 319-333.
- Reyniers, M., Walvoort, D. J., De Baardemaaker, J. 2006. A linear model to predict with a multi-spectral radiometer the amount of nitrogen in winter wheat. Int. J. Remote Sens. 27 (19), 4159-4179.
- Rondeaux, G., Steven, M., Baret, F. 1996. Optimization of Soil-Adjusted Vegetation Index. Remote Sens. Environ. 55, 95-107.
- Rouse, J. W., Haas, R. H., Schell, J. A., Deering, D. W. 1973. Monitoring vegetation systems in the Great Plains with ERTS. Third ERTS Symposium. NASA SP 351(I), 309-317.
- Samborski, S.M., Tremblay, N., Fallon, E. 2009. Strategies to make use of plant sensor- based diagnostic information for nitrogen recommendation. Agron. J. 101, 800-816.
- Thompson, R.B., Martínez-Gaitán, C., Gallardo, M., Giménez, C., Fernández, M.D. 2007. Identification of irrigation and N management practices that contribute to nitrate leaching loss from an intensive vegetable production system by use of a comprehensive survey. Agric. Water Manage. 89, 261-274.
- Thompson, R. B., Tremblay, N., Fink, M., Gallardo, M., Padilla, F. M. 2017. Tools and Strategies for Sustainable Nitrogen Fertilisation of Vegetable Crops. In: Tei, F., Nicola, S., Benincasa, P. (Eds.). Advances in Research on Fertilization Management of Vegetable Crops Part of the series Advances in Olericulture. Springer International Publishing. pp. 11-63
- Tremblay, N., Wang, Z., Cerovic, Z.G. 2012. Sensing crop nitrogen status with fluorescence indicators. A review. Agronomy for Sustainable Development 32, 451-464.
- Tucker, C.J. 1979. Red and photographic infrared linear combinations for monitoring vegetation. Remote Sens. Environ. 8, 127-150.
- Varco, J. J., Raper, T. B., Hubband, K. J. 2013. Canopy-Based Normalized Difference Vegetation Index Sensors for Monitoring Cotton Nitrogen Status. Agron. J. 105 (5), 1345-1354.
- Vogelmann, J. E., Rock, B. N., Moss, D. M. 1993. Int. J. Remote Sens. 14 (8), 1563- 1575.
- Xue, L. H., Cao, W. X., Luo, W. H., Dai, T. B., Zhu, Y. 2004. Monitoring leaf nitrogen status in rice with canopy spectral reflectance. Agron. J. 96, 135-142.
- Zhu, Y., Yao, X., Tian, Y. C., Liu, X. J., Cao, W. X. 2008. Analysis of common canopy vegetation indices for indicating leaf nitrogen accumulations in wheat and rice. Int. J. Appl. Earth Observ. Geoinf. 10, 1-10.