Serialización de DSCSA 2023 en Estados Unidos
Fecha límite de la Ley de Seguridad de la Cadena de Suministro de Medicamentos en EE UU: noviembre 2023
27 de noviembre de 2023, es la fecha límite de la FDA para el cumplimiento de la Ley de Seguridad de la Cadena de Suministro de Medicamentos (DSCSA) de Estados Unidos. La Ley de Seguridad de la Cadena de Suministro de Medicamentos (DSCSA), tiene como objetivo proteger el producto y al paciente mediante lo siguiente: Aumentar la capacidad de ayudar y proteger a los consumidores de la exposición a medicamentos que puedan ser falsificados, robados, contaminados o dañinos de cualquier otra forma y mejorar la detección y eliminación de medicamentos potencialmente peligrosos de la cadena de suministro de medicamentos.

Todas las partes interesadas del sector farmacéutico, tanto fabricantes como socios comerciales (reenvasadores, distribuidores, mayoristas y dispensadores), deberán disponer de una solución interoperable segura de seguimiento y localización para crear un sistema electrónico interoperable completo de seguimiento e identificación de los medicamentos con receta a la venta en Estados Unidos.
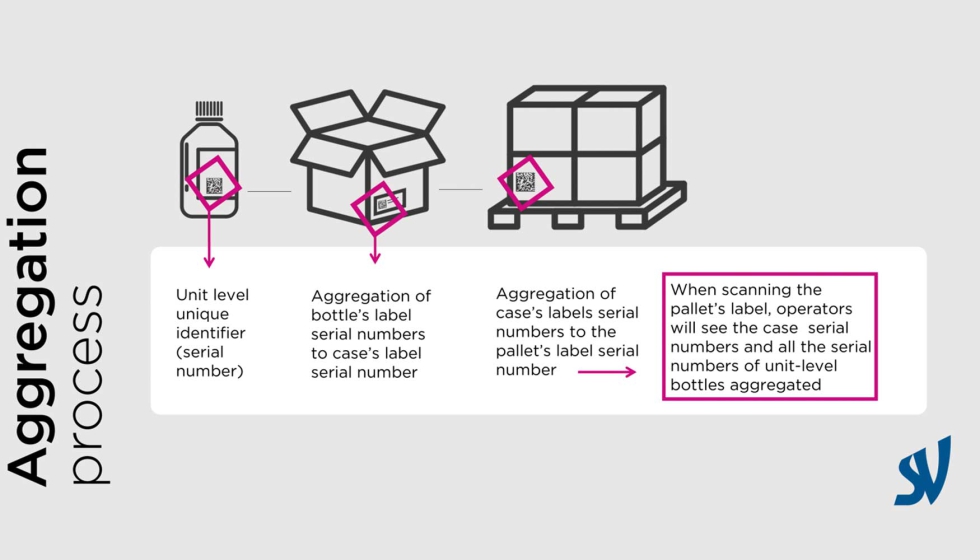
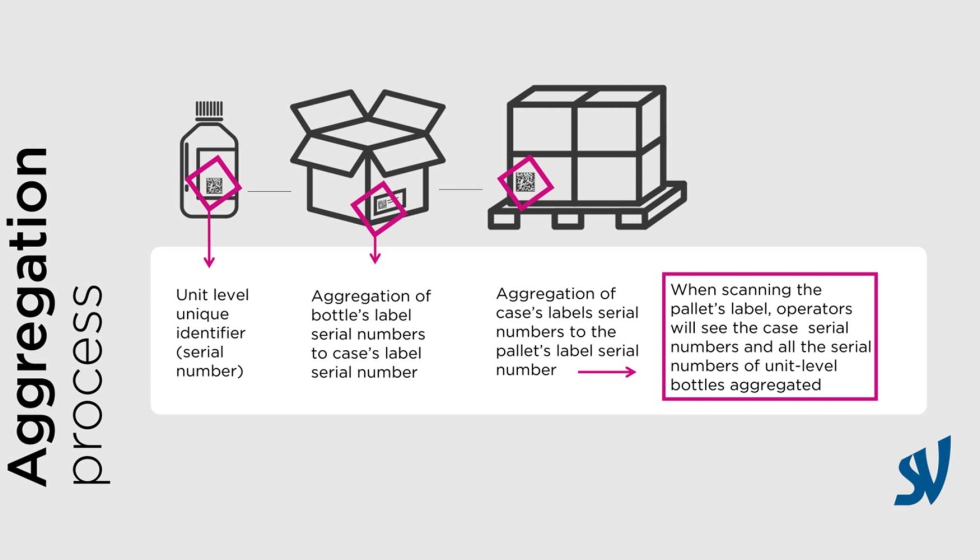
La agregación jerárquica permitirá identificar con precisión los artículos en la cadena de suministro y detectar más fácilmente cualquier producto falsificado. La agregación también proporcionará un mayor nivel de seguridad y visibilidad de los productos en la cadena de suministro de medicamentos, facilitando el intercambio de datos con los socios comerciales.
Panorama de la situación actual
La serialización es obligatoria por la FDA desde 2017 y requiere que todos los actores de la cadena de suministro de medicamentos se adhieran a los requisitos de trazabilidad, serializando los productos y verificando los números de serie. Para verificar los productos a nivel de envase dentro de toda la cadena de suministro, es necesario asignar y autenticar los números de serie en unidades individuales y en sus envases, empezando por los fabricantes hasta los reenvasadores, distribuidores y dispensadores.
Los fabricantes debían serializar y verificar los productos en el nivel de envase secundario (SKU). Tanto las unidades individuales como los envases contenían datos de serialización sin ninguna relación de parentesco entre ellos. Cuando el fabricante, mayorista o envasador envía los productos, debe transmitir a los socios comerciales la documentación 3T, que incluye el Historial de transacciones (TH), la Información de la transacción (TI) y el Extracto de la transacción (TS). Toda la información incluida en la documentación no proporciona la lista de números de serie enviados.
La ausencia de información jerárquica entre los expedidores y las unidades individuales suele ser la causa de que los operarios tarden mucho tiempo en gestionar las operaciones sencillas de reelaboración del almacén, como: envíos, envíos parciales, reempaquetado, muestreo.
Dado que el código impreso en la etiqueta del cargador no proporciona ninguna información sobre los números de serie de las unidades individuales almacenadas en su interior, para los socios comerciales que reciben mercancías de los fabricantes a menudo es difícil detectar la posición de cada unidad individual, ya que los productos se embalan en una unidad de cargador mayor que no está vinculada a los productos que contiene.
2023: mayor seguridad en la distribución de medicamentos
Con los nuevos requisitos establecidos por la DSCSA, los mayoristas y los dispensadores están obligados a implantar la trazabilidad interoperable y electrónica de los productos a nivel de envase, intercambiando datos (información de trazabilidad del producto, IT y TS) entre ellos. Además, si los distribuidores desean revender un producto devuelto, el fabricante debe poder recibir electrónicamente una consulta a la que responder con prontitud.
Esto puede ocurrir utilizando sistemas plenamente capaces de rastrear y verificar los productos distribuidos a lo largo de la cadena de suministro de la distribución farmacéutica.

Qué va a cambiar
En detalle, a partir del 27 de noviembre de 2023 la información sobre transacciones (IT) proporcionada por los fabricantes deberá incluir los datos PI (Product Identifier) a nivel de envase, que contendrán además el número de serie y la fecha de caducidad de cada producto.
Para los fabricantes esto significa que, para seguir vendiendo productos en la cadena de suministro, será necesario implantar un sistema de agregación, capaz de asociar los números de serie de cada producto (cajas de cartón) con su nivel superior de envasado (cajas y palés).
Ventajas de implantar un sistema de trazabilidad que cumpla los requisitos
Por poner otro ejemplo de las muchas ventajas que aporta este sistema, los reempaquetadores no tendrán que dedicar tiempo a retrabajar o escanear la unidad vendible, sino que sólo tendrán en cuenta (escanearán) la matriz que incluirá la información de todos los números de serie en su interior, ahorrando tiempo y reduciendo los errores humanos.
Cómo estar preparado para la DSCSA de EE.UU.
La relación de agregación física entre los expedidores padres y los envases secundarios o "hijos almacenados en su interior, y suele establecerse en un sistema electrónico durante las actividades de envasado y distribución del producto.
Para crear un sistema interoperable capaz de serializar, agregar y transmitir documentación electrónica, los fabricantes deben estar preparados para intercambiar datos con diferentes organizaciones, cada una con su propio sistema y formatos de datos.
Los requisitos mínimos para estar preparados pueden resumirse como sigue:
- Configuración de una solución completatodo en uno que asigne números de serie a cada producto desde las unidades individuales (cajas de cartón, botellas, viales, etc.) hasta los niveles superiores (expedidores/palés) y los vincule entre sí en una relación jerárquica.
- Configurar un software capaz de implementar un proceso fiable y un historial de transacciones de productos
- Ser capaz de manejar varios formatos de archivos de exportación como CSV, XML que cumplan con los estándares GS1 (por ejemplo, EPCIS 1.2).
- Ser capaz de manejar diversos protocolos de intercambio de datos, como SFTP.
- Configurar un software de sistema de rastreo interoperable capaz de intercambiar documentación 3T