Índice de Potencial Aromático varietal de uvas, mostos y vinos, blancos y tintos, determinación y automatización
Son numerosos los parámetros que influyen sobre el potencial aromático de las uvas, ya que no sólo están relacionados con la variedad vinífera sino que las condiciones edafoclimáticas y agronómicas en las que se desarrolla la planta1,2 repercuten sin duda en la calidad del vino obtenido3,4. Por todo ello, desde hace tiempo el sector vitivinícola ha demandado una herramienta para evaluar dicho potencial.
Potencial aromático: qué es y su importancia
La uva posee compuestos que contribuyen al aroma del vino que se encuentran tanto en forma de moléculas volátiles como en forma de precursores no olorosos. El potencial aromático en las uvas de vinificación está determinado predominantemente por los precursores glicosídicos. Estos constan de una molécula volátil (aglicona) unida a una glucosa mediante un enlace O-glicosídico, estando esta glucosa como tal o bien formando parte de un disacárido. Este enlace puede romperse a pH ácido o mediante la acción de enzimas con actividad glicosidásica, liberándose tanto la aglicona como la molécula de glucosa, a la que se conoce como glicosil-glucosa o glucosa G-G.
Estos precursores pasan al mosto durante el proceso de vinificación, en donde se produce la liberación de parte de sus agliconas tras romperse el mencionado enlace. Asimismo, durante la fermentación alcohólica y maloláctica, o incluso durante el embotellado y crianza del vino, esa liberación puede continuar. El conjunto de estos compuestos volátiles (agliconas) contribuyen al aroma varietal que percibe el consumidor de vino, y que es de gran importancia porque le aporta calidad y tipicidad. Además, es sabido que estas agliconas contribuyen de forma positiva al aroma, predominando las que se incluyen dentro de las familias de los terpenoles, norisoprenoides y bencenoides sobre la familia de los compuestos C65.

Cómo medir el potencial aromático
El potencial aromático de las uvas puede ser estimado de dos maneras, una de ellas determinado las agliconas volátiles liberadas y otra analizando la glucosa G-G, ya que existe una relación equimolecular precursor/glucosa/aglicona. Sin embargo, la determinación de las agliconas implica la cuantificación de muchos compuestos volátiles, mientras que la determinación de la glucosa G-G es una sola medida, lo cual simplifica la interpretación de los resultados. Por todo ello, la determinación de la glucosa G-G es la forma más rápida y sencilla para evaluar el potencial aromático de las uvas, lo que permite obtener una información útil para tomar decisiones a corto plazo en el sector productivo, en especial en bodegas.
Debido al interés por este parámetro, desde hace tiempo distintos autores han propuesto métodos para su determinación6-9, aunque presentaban importantes limitaciones ya que este análisis requiere la eliminación de las interferencias producidas por otros compuestos que también poseen enlaces O-glicosídicos con la glucosa, como ocurre en ciertos compuestos polifenólicos, en especial las antocianinas y los flavonoles. Las antocianinas son los compuestos glicosilados más abundantes en uvas tintas, y responsables de su color rojo y azulado. También en las uvas tintas y en las blancas hay flavonoles, cuyas concentraciones exceden generalmente a las de los precursores aromáticos glicosilados. Por tanto, es necesario eliminar estas interferencias polifenólicas antes de romper el enlace O-glicosídico, con el fin de que la glucosa G-G que se determine sea solo la que procede de los precursores aromáticos.
Los métodos de análisis anteriormente citados se basan en una extracción en fase sólida (SPE) del conjunto de compuestos glicosilados (aromáticos y polifenólicos) y la hidrólisis de los mismos. Pero quedaron sin resolverse los problemas de las interferencias polifenólicas, y el uso de patrones de referencia adecuados para el correcto seguimiento del análisis. Finalmente en 2012, Salinas y col.10 propusieron un método para la medida de la glucosa G-G que aborda con éxito los problemas anteriormente mencionados. En este trabajo se emplean cartuchos SPE con un nuevo material adsorbente que retiene los compuestos polifenólicos glicosilados, y a diferencia de los otros métodos se analiza la solución eluída, la cual está libre de interferencias, aunque contiene glucosa libre pero que es eliminada completamente sin influir en el contenido de los precursores aromáticos. Por tanto, este método consigue obtener una disolución en la que solo se encuentran los precursores aromáticos glicosilados; su posterior hidrólisis ácida nos permite conocer la glucosa G-G y por tanto el contenido de precursores de la muestra dada la relación equimolecular que hay entre ellos.
En relación al problema del patrón de referencia durante el análisis, se propone la utilización del β-D-fenilglucosa, compuesto que también ha sido seleccionado por otros autores cuando pretenden analizar oligosacáridos y otros glicósidos en vinos11.
No obstante, el método de Salinas y col. analiza la glucosa G-G mediante HPLC-IR y este equipo instrumental no está disponible en la mayoría de las bodegas. Con el objetivo de desarrollar una herramienta sencilla y mediante el empleo de equipos analíticos habituales en la mayoría de las bodegas, a partir de este trabajo y en colaboración con la empresa Teknokroma Analítica S.A., ha sido posible lanzar al mercado recientemente un kit que permite la determinación espectrofotométrica del contenido de glucosa G-G en uvas y vinos, tintos y blancos, mediante el parámetro denominado IPAv o Índice de Potencial Aromático varietal. Este parámetro requiere el empleo de todas las etapas analíticas del método de referencia, pero la determinación de la glucosa G-G es realizada por espectrofotometría UV-Vis. Esta técnica espectrofotométrica está disponible en la mayoría de las bodegas al ser requerida para muchas de las determinaciones analíticas clásicas que se llevan a cabo para el control de calidad de la uva y de las vinificaciones.
Por tanto, el IPAv es un nuevo parámetro que:
- Informa sobre la calidad aromática de la muestra mediante una espectrofotométrica.
- Mide la glucosa G-G de los precursores aromáticos glicosilados previamente aislados y sometidos a hidrólisis ácida.
- Permite evaluar la calidad aromática de forma global, mediante un único valor (índice).
- Es aplicable en uvas, mostos y vinos, blancos y tintos.
En muestras de uvas es necesaria la preparación previa de un extracto, mientras que en mostos y vinos basta con aplicar el kit IPAv (Teknokroma) a la muestra siguiendo el protocolo que se especifica.
Aplicaciones del IPAv como medida de potencial aromático
El IPAv hace una estimación global de las agliconas volátiles que están en forma de precursores y contribuyen de forma positiva al aroma, por lo que un mayor valor de este índice en muestras de uvas y mostos, indica mayor contenido de precursores y mayor posibilidad de que las agliconas se liberen. En el caso de los vinos, un mayor IPAv indica mayor potencial aromático de reserva, pudiendo producirse la liberación de agliconas con el paso del tiempo.
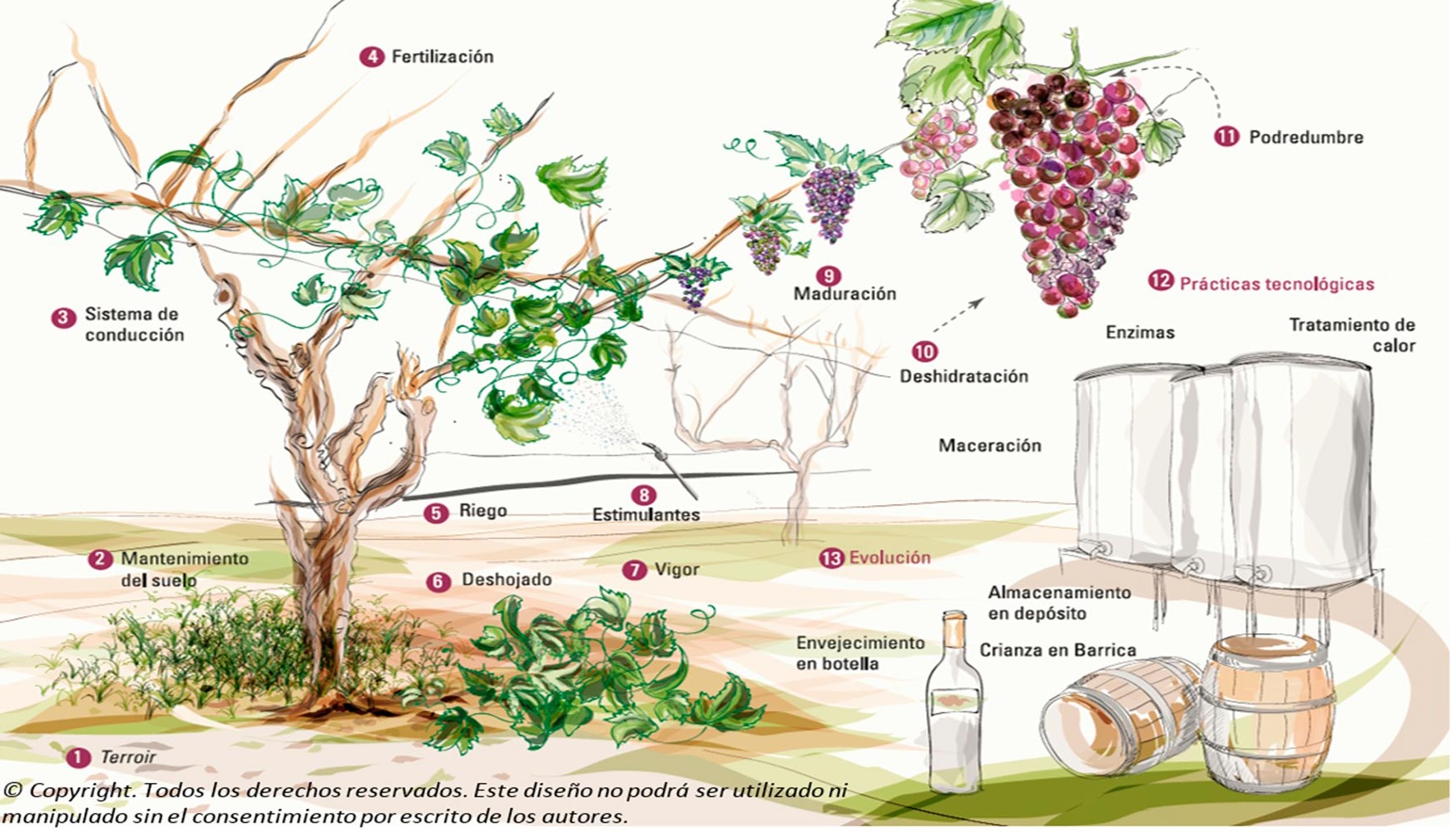
En base a lo anterior, se ha demostrado la utilidad y versatilidad del IPAv para conocer la influencia de determinadas prácticas agronómicas y enológicas en la calidad aromática de distintas variedades de uvas y de vinos, tanto blancos como tintos12. El estudio de la aplicabilidad de este método a mostos y vinos, en distintos momentos del proceso de elaboración y durante su evolución posterior, se recoge en uno de los bloques de la tesis doctoral citada, en la que parte de los trabajos realizados se llevaron a cabo en cooperación con bodegas de diversas regiones españolas. En la figura inferior se muestra el esquema gráfico con todas las aplicaciones en las que se ha evaluado el potencial aromático. Como se pone de manifiesto en la imagen, el parámetro IPAv permitió estudiar la influencia tanto de diversas actuaciones sobre la planta como las relacionadas con prácticas tecnológicas y posterior evolución del vino.
Parte de los resultados obtenidos por nuestro grupo de investigación quedan recogidos en diversos trabajos científicos5,16-19.
El IPAv ha despertado gran interés en el sector, tanto a nivel de bodegas como a nivel de otros grupos de investigación, que han incorporado este parámetro en diversos trabajos como forma de evaluar la calidad aromática en sus muestras13-15.
Además, algunos laboratorios referentes en el sector vitivinícola, lo han incorporado en su carta de servicios y los ofrecen a sus clientes, como es el caso de los Laboratorios Excell Ibérica, en Logroño.

Últimos avances en la determinación del IPAv
Durante los últimos años se ha continuado trabajando en el método IPAv con el objetivo de simplificarlo aún más y conseguir adaptarlo a las necesidades analíticas detectadas, que fundamentalmente requerían disminuir el tiempo de análisis y aumentar el número de muestras que podían realizarse simultáneamente. Para ello, la empresa Teknokroma a través de un proyecto CDTI y en colaboración con nuestro grupo de investigación, ha logrado adaptar el método hasta el punto de poder ser automatizado en gran parte de las etapas analíticas. Algunos de los resultados alcanzados han sido:
- La posibilidad de emplear multiplacas de 96 pocillos, que mejora significativamente tanto el tiempo de análisis como el número de muestras por día.
- La miniaturización, optimización y selección de la tecnología han posibilitado la integración de gran parte del procedimiento analítico para su automatización.
- La validación el concepto IPAv mediante ensayos en diversas bodegas, tanto en variedades tintas como blancas, y empleando todas las matrices posibles: uvas, mostos y vinos.
- La mejora el método de extracción para los precursores glicosilados de la uva, reduciendo el tiempo de preparación en este tipo de muestras.
- El diseño de un equipo que permite la automatización de la mayor parte de las etapas de análisis, pudiendo adaptarse al volumen demandado, versátil, cómodo y de sencillo manejo (fotografía inferior).
Referencias
- [1] Fragasso, M., Antonacci, D., Pati, S., Tufariello, M., Baiano, A., Forleo, L.R., La Notte, E. (2012). American Journal of Enology and Viticulture, 63, 477-486.
- [2] Martínez-Gil, A.M., Angenieux, M., Pardo-García, A.I., Alonso, G.L., Ojeda, H., Salinas, M.R. (2013). Food Chemistry, 138, 956-965.
- [3] Oliva, J., Garde-Cerdán, T., Martínez-Gil, A.M., Salinas, M.R., Barba, A. (2011). Food Chemistry, 129, 1676-1680.
- [4] Pardo-García, A.I., Serrano de la Hoz, K., Zalacain, A., Alonso, G.L., Salinas, M.R. (2014). Food Chemistry, 163, 258-266.
- [5] Salinas, M.R. & Serrano de la Hoz, K. (2012). Encuentros técnicos: Fundación para la cultura del vino, Madrid.
- [6] Iland, P.G., Cinkar, W., Francis, I., Williams, P.J., Coombe, B.G. (1996). Australian Journal of Grape and Wine Research, 2, 171178.
- [7] Whiton, S. & Zoecklein, B.W. (2002). American Journal of Enology and Viticulture, 53, 315-317.
- [8] Williams, P.J., Cynkar, W., Francis, I.L., Gray, J.D., Iland, P.G. Coombe, B.G. (1995). Journal of Agricultural and Food Chemistry, 43, 121-128.
- [9] Zoecklein B.W., Douglas L.S., Jasinski Y.W. (2000). American Journal of Enology and Viticulture, 51, 420-423.
- [10] Salinas, M.R., Serrano de la Hoz, K., Zalacain, A., Lara, J.F., Garde-Cerdán, T. (2012). Talanta, 89, 396-400.
- [11] Ruíz-Matute, A.I., Sanz, M.L., Moreno-Arribas, M.V., Martínez-Castro, I. (2009). Journal of Chromatography A, 1216, 7296-7300.
- [12] Serrano de la Hoz, K. (2014). Tesis Doctoral.
- [13] Álvarez, K., Tubio, M., Lissarrague, J.R., Zaldivar, E., Palacios, A. (2014). Enoviticultura nº 27, 6-21.
- [14] Álvarez, K., Tubio, M., Lissarrague, J.R., Palacios, A. (2014). Semana Vitivinícola nº 3.419, 326-333.
- [15] Crespo J., Romero V., García M., Arroyo T., Cabellos J.M. (2015). XIII Congreso Nacional de Grupos de Investigación Enológica (GIENOL), Tarragona.
- [16] Serrano de la Hoz, K., Carmona, M., Zalacain, A., Alonso, G.L., Salinas, M.R. (2014). 37 th World Congress of Vine and Wine, Mendoza, Argentina.
- [17] Serrano de la Hoz, K. & Salinas, M.R. (2014) Enólogos (www.revistaenologos.es)
- [18] Sánchez-Gómez, R., Zalacain, A., Serrano de la Hoz, K., Alonso, G.L., Salinas, M.R. (2015). XIII Congreso Nacional de Grupos de Investigación Enológica (GIENOL), Tarragona.
- [19] Serrano de la Hoz, K., Zalacain, A., Alonso, G.L., Salinas, M.R. (2015). FEAE, nº 1, 54-57.