Posibilidades en el tratamiento de residuos de pilas y baterías
13 de diciembre de 2011
Otros autores: María Dolores Murcia Almagro, Asunción María Hidalgo Montesinos y María Soledad Rojo García, de la Universidad de Murcia
Cuando una pila pierde su capa protectora quedan expuestos una serie de metales pesados que producen efectos notoriamente nocivos para el ecosistema y nuestra salud, entre los que figuran el zinc, cadmio, plomo y mercurio. Los residuos generados, cuando las pilas y baterías se han agotado, se clasifican según la nomenclatura establecida en la Orden MAM/304/2002, de 8 de febrero, por la que se publican las operaciones de valorización y eliminación de residuos y la Lista Europea de Residuos, así como en el Catálogo Europeo de Residuos.
Principales procesos para el reciclaje de pilas y baterías
Actualmente, los principales procesos utilizados en Europa para reciclar pilas y baterías una vez finalizada su vida útil se basan en técnicas hidrometalúrgicas y pirometalúrgicas.
Técnicas hidrometalúrgicas
Los métodos hidrometalúrgicos consisten en la disolución parcial o total de metales en agua con ácidos o bases fuertes y extracción selectiva de metales para su uso como materia prima en la industria metalúrgica [1]. Las etapas de este proceso son:
- Molienda: trituración de la masa de pilas previa selección y limpieza.
- Separación: tamizado que separa el polvo fino, separación magnética de materiales ferromagnéticos, como la carcasa de hierro, y de no ferromagnéticos, como las piezas de cinc, y separación neumática del papel y el plástico.
- Lixiviación: separación de los metales en la fracción de polvos finos, mediante tratamiento ácido y posterior neutralización para separar sales metálicas.
- Enriquecimiento: concentración de soluciones pobres por extracción líquido-líquido mediante disolventes orgánicos y al mismo tiempo purificación alcalina.
- Purificación: separación de sustancias acompañantes e impurezas por extracción sólido-líquido y/o precipitación (en forma de hidróxidos o sulfuros, cementación).
- Obtención: separación electrolítica del metal con ánodos insolubles (Zn, Cu).
- Refinación: separación electrolítica del metal con ánodos solubles (Cu, Pb) [2].

En los procesos indicados pueden aparecer las siguientes emisiones y materias brutas de relevancia ambiental:
- Agua residual: puede haber cantidades mayores o menores de metales pesados tóxicos para el ser humano y para las plantas.
- Residuos de lixiviación: contienen compuestos metálicos contaminantes.
- Gases de escape: niebla ácida y ácido sulfúrico aparecen en la electrólisis de obtención. Vapores que contienen metales, por ejemplo, en hornos con ánodo de cobre bruto. Disolventes orgánicos, por ejemplo, xerosina en la extracción líquido-líquido en el proceso de enriquecimiento.
- Fango de ánodos: en el fango aparecen metales y compuestos metálicos, por ejemplo, plata o plomo.
- Electrolito evacuado: contiene compuestos metálicos disueltos de hierro, níquel, cinc, arsénico y cobalto [1].
Técnicas pirometalúrgicas
Bajo la denominación de métodos pirometalúrgicos están aquellos que involucran la transformación y separación de componentes a partir de un tratamiento térmico del residuo en medio reductor (combustión con coque) y separación de los metales volátiles. Los procesos pirometalúrgicos son relativamente simples pero no versátiles y consumen grandes cantidades de energía en comparación con las técnicas hidrometalúrgicas [3]. Las etapas de un proceso pirometalúrgico son:
- Calcinación: desulfuración parcial o completa (calcinación total) del material de alimentación.
- Calcinación sinterizante: quemado del azufre con entrada de aire (transformación de los sulfuros en óxidos metálicos y gas SO2) con aglomeración simultánea del producto calcinado para la carga en hornos de cuba.
- Rotación del horno: enriquecimiento de óxido metálico mediante volatilización controlada (Zn).
- Fusión: separación de ganga (escorias); obtención de sulfuros metálicos de alto valor por combustión parcial del contenido de azufre o reducción de óxidos metálicos (PbO, ZnO) bajo combustión de coque con aportación de aire.
- Soplado: transformación de sulfuro metálico en metal en el convertidor.
- Refinación pirometalúrgica: eliminación, en las mezclas metálicas fundidas, del oxígeno, azufre, impurezas y metales acompañantes, por precipitación intermetálica, laboreo de escorias y/o volatilización.
- Empobrecimiento de escorias: procesamiento térmico de las escorias para obtener componentes metálicos [4].
En los procesos citados se producen numerosas emisiones y residuos:
- Gases de escape de diferente origen: polvo primario del material de alimentación; polvo de metales volátiles (plomo, cinc, cadmio, mercurio y sus compuestos (condensados después de enfriamiento), o sustancias gaseosas como SO2, HCl, HF, CO, CO2.
- Agua residual de circuitos de refrigeración y de lavados de gas de escape.
- Escorias finales con contenidos metálicos residuales, sulfatos y sulfuros.
- Desprendimiento del horno con contenido de plomo, cadmio, mercurio.
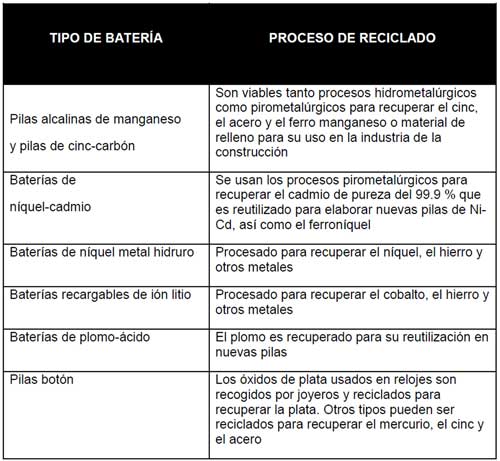
Por otro lado, cuando la tecnología para el reciclado de componentes no está disponible o involucra costos muy elevados, se utilizan procesos físico-químicos para disminuir significativamente la movilidad de los metales pesados. Estas técnicas incluyen: estabilización por agregado de agentes químicos que forman compuestos insolubles con los metales, confinamiento en envases herméticos, encapsulamiento con cemento, vitrificación a altas temperaturas, entre otras. Una vez tratado el residuo, generalmente se dispone en vertedero. Cuando se utiliza encapsulamiento con cemento, es recomendable colocar las pilas en un envase hermético con agregado de un reactivo básico para neutralizar los productos de alteración ácidos para preservar la estructura frente a ataques químicos [1]. En la Tabla 1 se muestran estos procesos de reciclado, de modo general, para cada tipo de pilas y baterías, según las fuentes de la EPBA.
Reciclaje de pilas y baterías en España
Experiencias de recuperación y reciclado de pilas y baterías en España
Las experiencias más frecuentes que se están llevando a cabo para la recuperación y reciclado de las pilas y baterías usadas en España según las fuentes del Programa Nacional de Pilas y Baterías Usadas (2007-2015) son las siguientes:
- Reciclado del cinc en pilas alcalinas y de cinc-carbón.
- Reciclado de pilas de níquel-cadmio.
- Reciclado de Hg de pilas de mercurio y plata de pilas botón.
- Reciclado de pilas estándar (alcalinas, salinas, etc.) por procedimiento hidrometalúrgico.
- Estabilización química de mezclas de pilas.
- Reciclaje de baterías de plomo-ácido.
Principalmente en nuestro país se reciclan las pilas botón, las pilas estándar y las baterías de plomo ácido pero las pilas de níquel-cadmio o de níquel-hidróxido de metal son enviadas a reciclar a otros países de la Unión Europea, como Francia, Alemania o Suiza, o fuera de esta comunidad, tal y como establece el Real Decreto 106/2008 en su artículo 12.

1. Reciclado del cinc en pilas alcalinas y de cinc-carbón
En primer lugar se realiza un proceso pirometalúrgico en el horno Waelz donde se obtiene el óxido Waelz, que se depura gracias a un segundo proceso hidrometalúrgico, obteniéndose así un óxido Waelz de elevada pureza y concentración en cinc. El proceso completo de reciclado se comenta con más detalle en apartados posteriores. El cinc se usa en la producción de acero galvanizado, que representa la mitad de su mercado. Un tercio del cinc consumido se produce a partir del reciclado del cinc usado [5].
2. Reciclado de pilas níquel-cadmio
Los procesos que se usan actualmente para este tipo de pilas en países desarrollados como Estados Unidos, Japón o países europeos consisten en técnicas pirometalúrgicas. Tenemos como ejemplo la experiencia de Saft, una importante industria mundial manufacturera de pilas y baterías, que las recicla cuando se agotan para hacer nuevas pilas de las mismas características [3].
En este proceso primero se realiza el desembalaje manual de las pilas. Se obtienen así las placas de níquel que se usan en la producción de acero; por otro lado se separa el plástico y el electrodo restante de cadmio se somete a un proceso térmico a 900 °C, donde se produce la evaporación de Cd, que se recupera posteriormente por condensación. Como residuo se obtiene hierro y níquel, que son enviados a la industria del acero para la fabricación del mismo. A diferencia de las baterías industriales, las pilas portátiles, antes de someterse al proceso térmico pasan por un tratamiento pirolítico. En el proceso de desmantelamiento, el agua utilizada es tratada para evitar al máximo el impacto ambiental nocivo [3].
Estos procesos pueden tener interés económico, al recuperar metales con una alta cotización. La pureza de recuperación del Cd es del 99,95%, siendo reutilizado para fabricar nuevas pilas o baterías de níquel-cadmio [6].
Algunos de los países que cuentan con instalaciones para la recuperación de este tipo de pilas son:
- Francia, con capacidad de 4.000 t/año.
- Suiza, con capacidad de 200 t/año.
- Japón, 3 plantas de 80 a 150 t/mes.
Uno de los principales inconvenientes de estas tecnologías es que requieren gran cantidad de energía, lo cual deriva en altos costos por lo que no resulta económicamente favorable en algunos países que deciden enviarlas a reciclar a otros países vecinos, como es el caso de España. Por otro lado, es un inconveniente la exigencia de una clasificación previa de estas pilas, la cual se realiza manualmente, si bien se están experimentando procesos de separación mecanizada, vía física o química [6].
3. Reciclado de mercurio y plata de pilas botón
El proceso consiste en liberar en forma de vapor el mercurio contenido en las pilas botón al someterlas, en una cámara de vacío, a baja presión y alta temperatura. El mercurio vaporizado pasa a una cámara de combustión, donde las partículas orgánicas se oxidan con oxígeno a temperaturas de 800 °C y posteriormente se condensa, mediante refrigeradores con aire forzado en un circuito cerrado de agua. Finalmente se extrae el mercurio por simple decantación y se somete a un proceso de afino, ya sea en la propia planta o en plantas externas.
Los residuos del horno se someten a una separación magnética, obteniendo chatarra reciclable y material no magnético, el cual es fundido obteniéndose plata y escoria de tipo vítreo con componentes potencialmente peligrosos. Esta operación se puede realizar en la planta de reciclaje de mercurio o en otras instalaciones especializadas en la recuperación de metales de los residuos del horno.
Los gases son depurados antes de su salida a la atmósfera, pasando por una columna de filtración con carbón activo [6]. Para que sea efectivo el proceso de reciclado de las pilas botón se han de cumplir los siguientes requerimientos:
- Obtención de contenidos residuales de mercurio del orden de ppm.
- No generar residuos con mercurio. La separación de componentes por métodos físicos no se considera aceptable.
- No deben generarse aguas residuales con mercurio disuelto, ya que requieren un tratamiento excesivamente costoso.
- El mercurio debe obtenerse en estado metálico para que pueda ser reciclado tras ser convenientemente afinado. De otro modo, el producto obtenido es, a su vez, un residuo.
El reciclado de las pilas botón de mercurio presenta como principal inconveniente el bajo precio del mercurio recuperado y los problemas que pueden ocasionarse si no son tratados adecuadamente los vapores de mercurio generados. La falta de viabilidad económica ha ocasionado el cese de operación de las plantas que trataban pilas botón en Alemania, Bélgica y Suiza [6].
4. Reciclado de pilas estándar (alcalinas, salinas, etc.) por procedimiento hidrometalúrgico
En líneas generales, recordemos, que los procesos hidrometalúrgicos constan de una primera etapa de trituración de las pilas, donde mediante procedimientos físicos se separan los elementos de encamisado de las pilas. La segunda fase consiste en atacar, mediante ácidos, la fracción salina de las pilas y recuperar los diferentes elementos metálicos por procesos físico-químicos en fase líquida ya que la mayoría de los metales existentes en las pilas son solubles en medios convencionales y, por tanto, pueden ser recuperados posteriormente o por separación selectiva y precipitación de sales o por deposición metálica en el cátodo de una célula electroquímica.
El sistema se caracteriza por su flexibilidad, es decir, por la posibilidad de ir adaptando el proceso según la composición de las pilas. El proceso es modular y permite llegar a la separación total de los metales después de la hidrólisis de los sólidos, o bien, realizar las operaciones intermedias necesarias para regenerar sólo ciertos metales [6].
Como principales ventajas del proceso podemos destacar las siguientes:
- Ausencia de emisiones de difícil y costosa descontaminación
- Ausencia de efluentes líquidos
- Pureza de metales
- Costes de implantación, explotación y consumo energético menores que los sistemas pirometalúrgicos
- Flexibilidad
- Recuperación de los metales que contienen las pilas.
5. Estabilización química de mezclas de pilas
Este proceso es aplicable a las pilas estándar y alcalinas. El proceso se sucede en tres fases perfectamente diferenciadas:
Fase de reacción, la cual se inicia con la preselección y trituración de las pilas en un reactor provisto de agitación, donde se mezcla la masa triturada con los agentes químicos estabilizantes que inducen la precipitación de determinados metales [6]. De este modo se consigue neutralizar los efectos nocivos de las pilas. Existen tres agentes estabilizantes que neutralizan el plomo, mercurio, cadmio y ácido sulfúrico, principales contaminantes de las distintas pilas que existen en el mercado [7].
Para el plomo actúa como agente neutralizador el sulfuro de sodio:
Na2S + Pb2+ → PbS + 2 Na+
Para el ácido sulfúrico, el agente estabilizante es hidróxido de sodio:
H2SO4 + Na(OH) → Na2SO4 + 2 H2O
Para el cadmio el agente estabilizante es el carbonato sódico:
Cd2+ + Na 2CO3 → CdCO3 + 2 Na2+
Para el mercurio se utiliza también sulfuro de sodio:
Hg2+ + Na2S → HgS + 2 Na2+
Fase de recuperación, mediante la absorción de los vapores amoniacales producidos sobre ácido sulfúrico, obteniéndose sulfato amónico de amplia utilización como fertilizante.
Fase de clasificación, mediante la cual se separa la masa inertizada de la chatarra que conforman las carcasas de las pilas, destinándose la chatarra a una posterior operación de reciclaje y depositando la masa inertizada en un vertedero de seguridad. El rendimiento obtenido tratando una mezcla de pilas salinas, alcalinas y botón está entre el 8-10 % de chatarra limpia y comercializable [6].

6. Reciclaje de baterías de plomo-ácido
España ha pasado de ser el primer productor mundial de plomo a carecer de metalurgia primaria del mismo. Por otra parte, el consumo, debido a la industria de la batería, se ha más que duplicado. La única producción nacional es la procedente del reciclado, que ha de ser completada con importaciones crecientes [8].
La producción primaria es la obtenida a partir de concentrados de plomo y supone una serie de etapas que se resumen a continuación:
Extracción del mineral: Consiste en el laboreo de la mina para extraer un mineral bruto que se somete a un tratamiento para conseguir concentrados ricos en plomo y con el mínimo contenido de otras sustancias.
Fusión: Reacción del concentrado con otros ingredientes para obtener el plomo bruto o ‘plomo de obra’, mediante: tostación oxidante de los sulfuros que pasan a óxidos o reducción de los óxidos en un horno de cuba, con adición de coque y otras sustancias para conseguir el plomo bruto. Existen otros procesos para obtener el plomo bruto en una sola etapa y que ofrecen ventajas desde el punto de vista de la economía energética y las emisiones (QSL, Kivcet, Isasmelt, TRBC).
Refino: necesario para purificar el plomo bruto, extrayendo del mismo las materias extrañas (Cu, Ni, As, Bi, Sb, Ag, Au, etc). El refino (o afino) se lleva a cabo en varias fases sucesivas, en calderas con adición de reactivos específicos en cada una de ellas. También puede refinarse el plomo bruto por vía electrolítica, usada generalmente para pequeñas capacidades.
Aleado: Mezcla del plomo refinado con otros metales para alcanzar una composición predeterminada [8].
Por otro lado, la producción secundaria es la que se obtiene a partir de chatarras o residuos plomíferos. A veces todo se reduce a una refusión de la materia prima secundaria con muy pocas operaciones complementarias, pero, cuando se trata de materias más complejas o de compuestos de plomo (las baterías desechadas, por ejemplo), hay que acudir a un proceso de fusión más complicado, que se complementa, generalmente, con el afino del plomo bruto obtenido en esa primera etapa. Los procesos a seguir son, en líneas generales, similares a los de la metalurgia primaria, aunque simplificados por basarse en materias primas de menor complejidad.
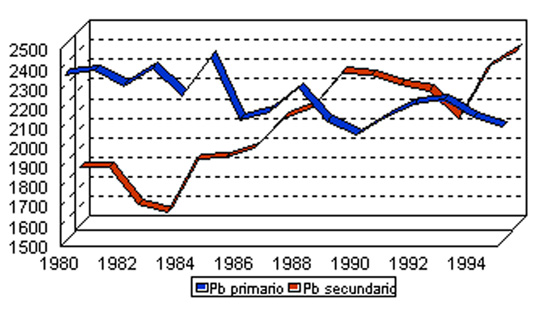
La producción secundaria necesita menos energía que la primaria (menos de la mitad). Se estima que el consumo energético para la metalurgia primaria es de 7.000 - 20.000 MJ/t y el de la secundaria de 5.000 - 10.000 MJ/t [8]. La proporción de plomo secundario en el conjunto mundial supera en varios puntos el 50% del plomo refinado total producido, siendo esta proporción aún mayor en los países más industrializados. EE UU y Europa Occidental producen, respectivamente, el 70% y el 60% de su plomo a partir de materias primas secundarias recicladas. Por el contrario, China basa su producción de metal casi exclusivamente en la minería. En la Figura 1 se puede ver cómo ha ido evolucionando en Europa Occidental la producción de plomo hasta el año 1994. Es el inicio de la disminución del plomo primario y el aumento del plomo secundario [9].
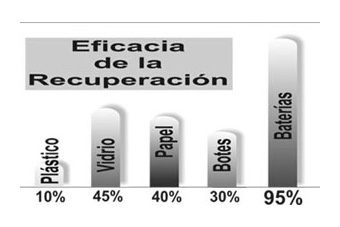
El índice de recuperación de baterías es, en Occidente, superior al 90%, alcanzándose en España una recuperación del 95–97%; por lo que es muy poco el plomo que queda sin ser recuperado y reciclado. Son éstos unos índices de recuperación posiblemente no alcanzados por ningún otro metal o compuesto, como refleja la Figura 2, que ilustra los niveles de reciclaje de diversos productos en España [10].
[2] Impactos Ambientales y Actividades Productivas. Etapas del proceso hidrometalúrgico. Estrucplan On Line – Salud, seguridad y medio ambiente en la industria. Disponible en Internet: http://www.estrucplan.com.ar/Producciones/imprimir.asp?IdEntrega=168
[3] Morales, L.T. (2004). Desarrollo de una propuesta para la construcción de una planta de reciclado de baterías de Ni-Cd por vía hidrometalúrgica. Tesis de la Universidad de las Américas, Puebla, Méjico.
[4] Impactos Ambientales y Actividades Productivas. Etapas del proceso pirometalúrgico. Estrucplan On Line – Salud, seguridad y medio ambiente en la industria. Disponible en Internet: http://www.estrucplan.com.ar/Producciones/imprimir.asp?IdEntrega=167
[5] Cinc. Disponible en Internet: http://es.wikipedio.org/wiki/Zinc
[6] Plan Nacional Integrado de Residuos (2007-2015). Anexo 8. Actualización del Programa Nacional de Pilas y Baterías Usadas.
[7] Díaz Díez, M.A.; Díaz Parralejo, A.; Macías García, A. y Sánchez-Marín Pizarro, J.M. Reciclado de materiales. Área de ciencias de materiales. Universidad de Extremadura. Disponible en Internet: http://dialnet.unirioja.es/servlet/fichero_articulo?codigo=1075308
[8] Uniplom (2003). Unión de Industrias del Plomo. Disponible en Internet:
http://www.confemetal.es/uniplom
[9] Gómez Gómez, J.M. El diseño y la abundancia: determinantes de la posibilidad de reciclado. Un ejemplo: pilas y baterías. Perdigones Azor S.A.
[10] Bañeres Sorinas, M. (2003). Estudio de alternativas en el reciclaje de baterías de plomo fuera de uso. Departamento de Ingeniería Química. Universidad Politécnica de Cataluña. Disponible en Internet: http://upcommons.upc.edu/pfc/bitstream/2099.1/3095/1/31396-1.pdf