Un encuentro con directivos de la sanidad organizado por Sedisa, con el apoyo de Farmaindustria, aborda las claves del desarrollo de los ensayos clínicos
La investigación clínica española acorta distancias con los mejores centros europeos
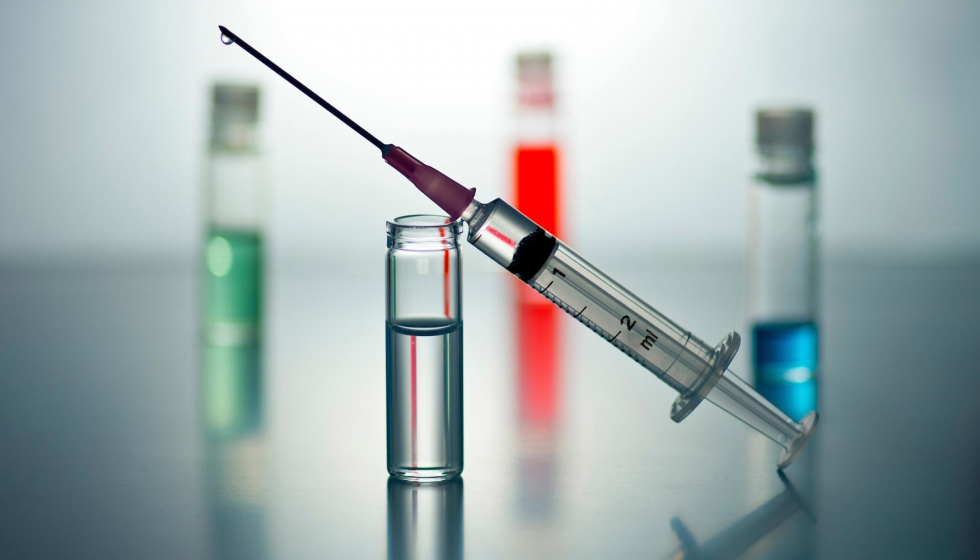
Para seguir avanzando, es fundamental que los directivos incorporen la investigación clínica de forma estratégica en la gestión sanitaria en todos los niveles asistenciales. “La mejora de la investigación clínica requiere plantear cambios organizativos que afecten a la asistencia sanitaria, a la propia investigación en los hospitales y a la enseñanza de la medicina”, explica Modoaldo Garrido Martín, vicepresidente primero de la Sociedad Española de Directivos de la Salud (Sedisa). “Además, conlleva el impulso de institutos o clúster que atiendan a grupos homogéneos de pacientes, lo que facilitaría la colaboración de los clínicos con los investigadores básicos y el enfoque multidisciplinar y el avance en investigación traslacional”.
Respecto a la organización de la investigación en los hospitales, el vicepresidente primero de Sedisa apunta que “es clave priorizar las líneas de investigación apoyando su desarrollo con los recursos necesarios y el impulso de las unidades de apoyo a la investigación, en las que trabajen epidemiólogos, bioestadísticos, farmacólogos clínicos, administrativos y gestores. Se trata de una responsabilidad directiva”.
Estos son algunos de los datos e ideas puestos de manifiesto este viernes en un encuentro organizado por Sedisa, con el apoyo de Farmaindustria, bajo el título ‘El futuro de la investigación clínica en España’. El encuentro es el primero que se celebra en virtud del acuerdo de colaboración suscrito por ambas entidades para promover la investigación, la difusión y la transferencia del conocimiento en el campo de los medicamentos y de la gestión de los servicios sanitarios y sociosanitarios.
En este sentido, durante el encuentro se puso de relieve que el plazo medio para la puesta en marcha de un ensayo clínico en España, desde que se presenta la documentación a las autoridades reguladoras y comités de ética hasta que se incluye al primer paciente, es actualmente de 174 días, según los últimos datos disponibles, correspondientes a 2016, lo que supone una reducción del 29% respecto al plazo de 244 días correspondiente a 2004.
César Hernández, jefe del Departamento de Medicamentos de Uso Humano de la Agencia Española de Medicamentos y Productos Sanitarios, puso de relieve los efectos positivos que ha tenido el reciente Real Decreto de Ensayos Clínicos, aprobado a finales de 2015, para situar a España en una posición de ventaja a la hora de aplicar el Reglamento europeo en esta materia, que entre otras cosas establece una evaluación única de cada ensayo clínico para toda Europa. En España se autorizan cada año unos 800 ensayos clínicos.

Amelia Martín Uranga, responsable de la Plataforma de Medicamentos Innovadores de Farmaindustria, indicó que desde 2004 y hasta el pasado año las compañías farmacéuticas han impulsado en España más de 7.200 ensayos clínicos, de los que la mitad corresponden a fases tempranas de la investigación (I y II), las que suponen una mayor complejidad y hacen posible además el acceso temprano de los pacientes a las nuevas terapias. Asimismo, según los datos del Proyecto BEST, en torno al 50% de estos estudios se centró en el descubrimiento y desarrollo de nuevos fármacos antitumorales.
Incremento de la investigación en Madrid
Esta primera jornada desarrollada en el marco de colaboración entre Sedisa y Farmaindustria se centró en la investigación clínica en la Comunidad de Madrid. En ella se puso de manifiesto la importancia de esta Comunidad en el mapa de la I+D de nuevos medicamentos en España, así como la tendencia al alza experimentada en los últimos años, como lo demuestra el porcentaje de ensayos clínicos con Comités Éticos de Referencia en Madrid, que ha pasado del 27,5% del periodo 2004-2009 al 42,3% en 2015-2016.
Asimismo, las participaciones de centros madrileños en ensayos clínicos es ya del 26,5%, frente al 22,3% de 2004-2009, una tendencia que se acentúa en el caso de las fases tempranas de la investigación, donde se ha pasado del 23,1% al 32,3%. Además, en los últimos años se ha incrementado el porcentaje de ensayos clínicos en Madrid que tienen participación de algún centro privado, que ya es cercano al 50%. Los ocho institutos de investigación sanitaria y las 11 fundaciones de investigación existentes en la Comunidad configuran una red muy atractiva para que la industria farmacéutica intensifique todavía más su apuesta en I+D en esta región.